|
|
Понятие о теории переходного состояния. Активированный комплекс.Энергия активации всегда меньше энергии, которую надо затратить, чтобы разрушить связи в молекулах исходных веществ. Это объясняет теория переходного состояния. На основании этой теории для протекания реакции необязательно полностью разрывать химические связи в исходных веществах, достаточно их ослабить. Это происходит при образовании промежуточного соединения – активированного комплекса. Пример: Реакция синтеза йодистого водорода.
Активные молекулы Н2 и I2 объединяются в промежуточный активный комплекс Н2¼I2, в котором образование новых связей Н–I идёт одновременно с разрывом связей Н–Н и I–I. Образование переходного состояния – процесс энергетически более выгодный, чем полное разрушение связей в молекулах исходных веществ. Вот почему образование активированных комплексов характерно для многих реакций, особенно ферментативных.
4. Катализ и катализаторы. В.И.Слесарев. «Химия. Основы химии живого». стр. 106-107.
Ферментативный катализ и его особенности. Все биохимические процессы протекают в присутствии катализаторов – ферментов. Ферменты – это белковые молекулы, которые катализируют химические реакции в живых организмах. Другое название ферментов – энзимы. В настоящее время известно около 2000 различных ферментов, около 150 ферментов удалось выделить в чистом виде. Для веществ, участвующих в ферментативных реакциях приняты следующие названия: · субстрат (S) – вещество, на которое фермент оказывает специфическое каталитическое действие; · фермент (Е) – вещество, ускоряющее превращение субстрата; · продукт (Р) – вещество, в которое превращается субстрат в результате ферментативного катализа.
Ферментативный катализ имеет свои особенности, отличающие его от обычного химического катализа: ü Высокая эффективность. Реакции, катализируемые ферментами, ускоряются в десятки тысяч раз. Объясняется это тем, что при действии фермента на субстрат образуется фермент-субстратный комплекс, энергия активации которого значительно ниже энергии активации некаталитической реакции.
ü Высокая специфичность (избирательность).Каждый фермент катализирует только определенную биохимическую реакцию, т.е. действует только на определенный субстрат. Для объяснения такой высокой специфичности используется теория «ключ-замок» или «рука-перчатка». В.И. Слесарев «Химия. Основы химии живого», стр.117-118. На активность ферментативного катализа влияют следующие факторы: § концентрация фермента § концентрация субстрата § температура § реакция среды (рН) В.И.Слесарев «Химия. Основы химии живого», стр.116-119.
Химическое равновесие. Химическое равновесие возникает в обратимых реакциях. Обратимыми называются реакции, которые протекают в двух взаимно противоположных направлениях. Например: Прям Н2 + J2 ⇄ 2НJ Обр Таких реакций большинство. Составим кинетические уравнения прямой и обратной реакций. uпр = k1·cH2·cJ2 uобр = k2·c2HJ
Состояние системы, при котором скорость прямой реакции равна скорости обратной называется химическим равновесием . uпр = uобр В условиях равенства скоростей, концентрации исходных веществ и продуктов реакции не изменяются, остаются постоянными и являются равновесными. Тогда, можно записать k1·cH2·cJ2= k2·c2HJ Для количественной характеристики состояния равновесия введен безразмерный параметр – константа равновесия. Она равна отношению констант скоростей прямой и обратной реакций.
Константа химического равновесия обратимого процесса прямо пропорциональна произведению концентраций продуктов реакции и обратно пропорциональна произведению равновесных концентраций исходных веществ, возведенных в степень равную их стехиометрическим коэффициентам. Кх.р. зависит от природы реагентов и температуры, но не зависит от концентраций и наличия катализатора. Значение константы определяет преимущество протекания одной из противоположных реакций: Если К > 1, то в системе выше содержание продуктов, т.е. преимущественно идет прямая реакция. Если К < 1, то в системе выше концентрация исходных веществ и преимущество имеет обратная реакция. Между константой равновесия и энергией Гиббса существует математическая зависимость:
R – газовая постоянная T – температура Kравн – константа равновесия.
Химическое равновесие носит динамический характер и характеризуется постоянством при неизменности внешних условий. При изменении концентрации реагентов, температуры и давления скорость одной из реакций может увеличиться, тогда происходит смещение равновесия: · если возрастает скорость прямой реакции, то равновесие смещается вправо; · если увеличится скорость обратной реакции, то равновесие смещается влево.
Смещение равновесия определяется принципом Ле-Шателье:
ü Влияние концентрации. При увеличении концентрации исходных веществ равновесие смещается вправо, а при увеличении концентрации продуктов реакции – влево.
ü Влияние температуры. При повышении температуры равновесие смещается в сторону эндотермической реакции, а при понижении температуры – в сторону экзотермической реакции.
ü Влияние давления (только для газов и при условии, что количество моль газов исходных веществ и продуктов не равны). При увеличении давления равновесие смещается в сторону реакции, которая протекает с уменьшением числа моль газов, а при уменьшении давления – в сторону увеличения числа моль газов. 12 |
|


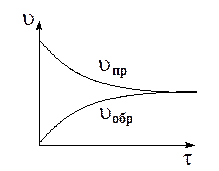 В обратимых реакциях скорость прямой и обратной реакций по-разному изменяются с течением времени. Так, в начальный момент времени скорость прямой максимальна, а скорость обратной реакции практически равна 0, т.к. продукты еще не образованы, а концентрация исходных веществ максимальна. С течением времени скорость прямой реакции будет убывать, а скорость обратной реакции увеличиваться пока не наступит их равенство.
В обратимых реакциях скорость прямой и обратной реакций по-разному изменяются с течением времени. Так, в начальный момент времени скорость прямой максимальна, а скорость обратной реакции практически равна 0, т.к. продукты еще не образованы, а концентрация исходных веществ максимальна. С течением времени скорость прямой реакции будет убывать, а скорость обратной реакции увеличиваться пока не наступит их равенство.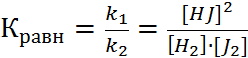
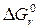 = – RT ln Kравн
= – RT ln Kравн
 Если на систему, находящуюся в равновесии оказать внешнее воздействие, то равновесие смещается в сторону той реакции, которая ослабит это воздействие.
Если на систему, находящуюся в равновесии оказать внешнее воздействие, то равновесие смещается в сторону той реакции, которая ослабит это воздействие.