|
|
Занятие 3. Теория Бора для атома водорода и водородоподобных атомов. Спектральные серии атома водорода.Краткие теоретические сведения Основные формулы Уравнение Шредингера для стационарных состояний в сферических координатах:
где В атоме водорода (водородоподобном ионе) потенциальная энергия
где Собственное значение энергии:
где Символическая запись
где Вероятность
где В Нормированные собственные
или в атомных единицах
где в качестве единицы длины принят боровский радиус:
При таком выборе единицы длины расстояние от ядра Вероятность
Орбитальные момент импульса и магнитный момент электрона:
где Проекции орбитальных момента импульса и магнитного момента на направление внешнего магнитного поля (совпадающего с осью
Гиромагнитное отношение для орбитальных магнитного и механического моментов:
Спин и спиновый магнитный момент электрона:
где Проекции спиновых момента импульса и магнитного момента на направление внешнего магнитного поля (совпадающего с осью
где Гиромагнитное отношение для спиновых магнитного и механического моментов:
Распределение электронов по состояниям в атоме с помощью спектроскопических символов:
Принцип Паули. В атоме не может находиться два (и более) электрона, характеризуемых одинаковым набором четырех квантовых чисел: Полный орбитальный момент импульса электрона: Полный орбитальный момент атома: Полный спиновый момент атома: Полный момент импульса атома: Символическое обозначение состояния атома (спектральный терм):
Энергия атома в магнитном поле: Правила отбора для квантовых чисел
Не осуществляются переходы Первый постулат Бора: движение электронов по стационарным орбитам не сопровождается излучением электромагнитных волн. В стационарном состоянии атома электрон, двигаясь по круговой орбите, должен иметь дискретные квантованные значения момента импульса, удовлетворяющие условию:
где Радиус стационарной орбиты атома водорода:
где Второй постулат Бора (правило частот): при переходе электрона с одной стационарной орбиты на другую излучается (поглощается) один фотон с энергией:
равной разности энергий соответствующих стационарных состояний Кинетическая, потенциальная и полная энергия электрона на орбите соответственно равны:
Момент импульса электрона на стационарных орбитах:
где Энергия электрона в водородоподобном атоме:
где знак минус означает, что электрон находится в связанном состоянии, Сериальная формула, определяющая длину волны
где Энергия фотона, испускаемого атомом водорода при переходе из одного стационарного состояния в другое,
где Вопросы для ответа у доски 1. Модель атома Томсона. 2. Рассмотрите случай рассеяния альфа-частиц на ядре атома. 3. В чем суть и результаты опытов Резерфорда? 4. Планетарная модель атома Резерфорда. 5. Сформулируйте постулаты Бора. 6. Изложите суть опытов Франка и Герца. 7. Рассчитайте энергию и радиусы орбит стационарных состояний водородоподобных систем. 8. Что такое энергия и потенциал ионизации атома? 9. Запишите и объясните формулы для серий спектральных линий Бальмера, Лаймана, Пашена, Брэкета. Примеры решения задач Задача 1. Вычислить радиус первой орбиты атома водорода и скорость электрона на этой орбите. Решение. Согласно теории Бора, радиус
Так как в задаче надо определить величины, относящиеся к первой боровской орбите, то главное квантовое число
Для определения двух неизвестных величин
Тогда, решая совместно два равенства, получаем:
Подставив сюда значения
Для скорости:
Ответ: Задача 2. Вычислить полную энергию электрона, находящегося на второй орбите атома водорода. Решение. Энергия электрона, находящегося на второй орбите атома, равна
Ответ: Задача 3. При переходе электрона с некоторой орбиты на вторую, атом водорода испускает свет с длиной волны 4,34·10-7 м. Найти номер неизвестной орбиты. Решение. Воспользуемся формулой для определения длины волны света, излучаемого атомом водорода при переходе с одной орбиты на другую:
Ответ: 5. Задача 4. Определить энергию фотона, соответствующую второй линии испускания в инфракрасной серии (Пашена) атома водорода при переходе на третий энергетический уровень. Решение. При переходе электронов с орбиты n >1 на орбиту m=1 получается серия Лаймана спектральных линий, лежащих в ультрафиолетовой области. При переходе электронов с орбит n >2 на орбиту m=2 получается серия Бальмера спектральных линий, лежащих в видимой области. При переходе электронов с орбит n >3 на орбиту m=3 получается серия Пашена спектральных линий, лежащих в инфракрасной области. Первая линия этой серии, получается при переходе электрона с орбиты n=4 на орбиту m=3. Вторая линия этой серии соответствует n=5, m=3. Тогда энергия фотона, соответствующая этой линии:
Ответ: Задача 5.Определить частоту света, излучаемого возбужденным атомом водорода, при переходе электрона на второй энергетический уровень, если радиус орбиты электрона изменится в 9 раз. Решение. Согласно обобщенной формуле Бальмера, частота света, излучаемого атомом водорода:
где R- постоянная Ридберга,
Электрон движется по орбите радиусом
Из теории Бора момент импульса электрона, движущегося по орбите:
умножим обе части (1) на
где По условию задачи Зная отношение радиусов орбит электрона при переходе с орбиты
Ответ: Задача 6. Определить энергию фотона, излучаемого атомом водорода при переходе электрона с третьего энергетического уровня на первый, а также длину электромагнитной волны, соответствующую этому фотону. Решение. Переход электрона в атоме водорода с отдаленной орбиты на внутреннюю связан с излучением фотона (кванта энергии):
где Длина волны излучаемого света связана с номером орбит соотношением:
где Подставляя числовые, находим длину волны:
Ответ: Вопросы и задания для самопроверки 1. Модель атома Томсона. 2. В чем суть и результаты опытов Резерфорда? 3. Планетарная модель атома Резерфорда. 4. Почему ядерная модель атома оказалась несостоятельной? В чем заключаются недостатки статической ядерной модели атома? 5. Сформулируйте постулаты Бора. Как с их помощью объясняется линейчатый спектр атома? 6. Какие основные выводы можно сделать на основании опытов Франка и Герца. 7. Достоинства и недостатки теории Бора. 8. Сформулируйте и объясните принцип соответствия. 9. Что такое энергия и потенциал ионизации атома? Как их рассчитать для атома водорода? 10. Определение спектра данной физической: величины. Приведите примеры. 11. Что называется спектром испускания и поглощения? Как они возникают? 12. Линейчатый спектр. Как он образуется? 13. Что такое полосатый спектр? Как он образуется? 14. Какой спектр называется сплошным и как он возникает? 15. Пользуясь моделью Бора, укажите спектральные линии, которые могут возникнуть при переходе атома водорода в состояния с 16. Нанесите на шкалу длин волн три линии каждой из двух спектральных серий атома водорода. 17. Что называется спектральной серией? 18. Почему из различных серий спектральных линий атома водорода первой была изучена серия Бальмера? 19. Какой смысл имеют числа 20. Чему равна частота излучения атома водорода, соответствующая коротковолновой границе серии Брэкета? 21. Почему спектр поглощения атома водорода содержит только серию Лаймана? Задачи для самостоятельного решения 1. Найти кинетическую 2. Найти период обращения электрона на первой боровской орбите атома водорода и его угловую скорость. 3. Какие спектральные линии появятся при возбуждении атомарного водорода электронами с энергией 12,5 эВ? 4. Какую наименьшую энергию нужно сообщить электрону, находящемуся на первой орбите в атоме водорода, чтобы электрон удалился в бесконечность. 5. Найти наибольшую и наименьшую длины волн в видимой области спектра излучения атома водорода. 6. Электрон в атоме водорода перешел с четвертого энергетического уровня на второй. Определить длину волны испускаемого фотона. 7. Какая частота электромагнитной волны, излучаемой атомом водорода, при переходе электрона с четвертого энергетического уровня на третий? 8. Определить энергию фотона, излучаемого атомом водорода при переходе электрона с третьего энергетического уровня на первый, а также длину электромагнитной волны, соответствующую этому фотону. 9. Вычислить для основного состояния атома водорода радиус круговой орбиты электрона и его скорость. 10. При переходе электрона в атоме водорода с одной орбиты на другую, более близкую к ядру, энергия атома уменьшилась на 1,892 эВ. Определить длину волны излучения. 11. При переходе электрона в атоме водорода с четвертого энергетического уровня на второй излучается фотон, дающий зеленую линию в спектре водорода. Определить длину волны этой линии, если атом теряет при излучении энергию 2,53 эВ. 12. Какую наименьшую энергию нужно сообщить электрону, находящемуся на первой орбите в атоме водорода, чтобы электрон удалился в бесконечность. 13. Найти наибольшую и наименьшую длины волн в видимой области спектра излучения атома водорода. 14. Электрон в атоме водорода перешел с четвертого энергетического уровня на второй. Определить длину волны испускаемого фотона. 15. Какая частота электромагнитной волны, излучаемой атомом водорода, при переходе электрона с четвертого энергетического уровня на третий? 16. Определить энергию фотона, излучаемого атомом водорода при переходе электрона с третьего энергетического уровня на первый, а также длину электромагнитной волны, соответствующую этому фотону. 17. Найти наименьшую 18. Найти наибольшую длину волны 19. Какую наименьшую энергию 20. В каких пределах должна лежать энергия бомбардирующих электронов, чтобы при возбуждении атомов водорода ударами этих электронов спектр водорода имел только одну спектральную линию? 21. Какую наименьшую энергию 22. В каких пределах должны лежать длины волн 23. На сколько изменилась кинетическая энергия электрона в атоме водорода при излучении атомом фотона длиной волны 24. В каких пределах должны лежать длины волн 25. Какие спектральные линии появятся при возбуждении атомарного водорода электронами с энергией 12,5 эВ? 26. Какую наименьшую энергию нужно сообщить электрону, находящемуся на первой орбите в атоме водорода, чтобы электрон удалился в бесконечность. 27. Найти наибольшую и наименьшую длины волн в видимой области спектра излучения атома водорода. 28. Электрон в атоме водорода перешел с четвертого энергетического уровня на второй. Определить длину волны испускаемого фотона. 29. Какая частота электромагнитной волны, излучаемой атомом водорода, при переходе электрона с четвертого энергетического уровня на третий? 30. Определить энергию фотона, излучаемого атомом водорода при переходе электрона с третьего энергетического уровня на первый, а также длину электромагнитной волны, соответствующую этому фотону. 31. Вычислить для основного состояния атома водорода радиус круговой орбиты электрона и его скорость. 32. При переходе электрона в атоме водорода с одной орбиты на другую, более близкую к ядру, энергия атома уменьшилась на 1,892 эВ. Определить длину волны излучения. 33. При переходе электрона в атоме водорода с четвертого энергетического уровня на второй излучается фотон, дающий зеленую линию в спектре водорода. Определить длину волны этой линии, если атом теряет при излучении энергию 2,53 эВ. 34. Какую наименьшую энергию нужно сообщить электрону, находящемуся на первой орбите в атоме водорода, чтобы электрон удалился в бесконечность. 35. Электрон в атоме водорода перешел с четвертого энергетического уровня на второй. Определить длину волны испускаемого фотона. 36. Какая частота электромагнитной волны, излучаемой атомом водорода, при переходе электрона с четвертого энергетического уровня на третий? 37. Определить энергию фотона, излучаемого атомом водорода при переходе электрона с третьего энергетического уровня на первый, а также длину электромагнитной волны, соответствующую этому фотону. 38. Определить, сколько различных волновых функций соответствует главному квантовому числу 39. Построить и объяснить диаграмму, иллюстрирующую расщепление энергетических уровней и спектральных линий (с учетом правил отбора) при переходах между состояниями с 40. Электрон в атоме находится в 1.4. Теоретические вопросы к модулю I. 1. В чем суть и каковы результаты опытов Бибермана, Сушкина и Фабриканта с электронными пучками малой интенсивности? 2. Изложите суть и основные выводы мысленного эксперимента по рассеянию электронов на двух щелях. 3. Как понимать утверждение, что волны де Бройля имеют вероятностный характер? 4. Чему равны фазовая и групповая скорости фотона? 5. Физический принцип работы электронного и ионного микроскопов. 6.Что называется динамическими переменными? 7. Почему динамические переменные не могут быть приписаны микрообъектам? 8. Что такое неопределенность данной физической величины? 9. В каком случае и почему при условиях 10. Надо ли учитывать волновые свойства 11. Как, исходя из соотношения неопределенностей, объяснить наличие естественной ширины спектральных линий? 12. Каким свойствам должна удовлетворять волновая функция? 13. Записать уравнения Шредингера для стационарных состояний электрона, находящегося в атоме водорода. 14. Временная часть уравнения Шредингера имеет вид 15. Что определяет квадрат модуля волновой функции? 16. Что называется собственными значениями энергии и собственными функциями? 17. Какие состояния называются вырожденными? Что такое кратность вырождения? 18. В чем заключается физический смысл волновой функции? 19. Как рассчитать момент импульса и его проекцию на полярную ось в случае системы частиц? 20. Как обозначают и называют состояние электрона с разными орбитальными квантовыми числами? 21. Сопоставьте боровскую теорию атома водорода с квантово-механической теорией. 22. Как изменится коэффициент прозрачности потенциального барьера с увеличением его ширины в два раза? 23. Может ли частица находиться на дне «потенциальной ямы»? Определяется ли это формой «ямы»? 24. Модель атома Томсона. 25. В чем суть и результаты опытов Резерфорда? 26. Планетарная модель атома Резерфорда. 27. Почему ядерная модель атома оказалась несостоятельной? В чем заключаются недостатки статической ядерной модели атома? 28. Сформулируйте постулаты Бора. Как с их помощью объясняется линейчатый спектр атома? 29. Какие основные выводы можно сделать на основании опытов Франка и Герца. 30. Достоинства и недостатки теории Бора. 31. Сформулируйте и объясните принцип соответствия. 32. Что такое энергия и потенциал ионизации атома? Как их рассчитать для атома водорода? 33. Определение спектра данной физической: величины. Приведите примеры. 34. Что называется спектром испускания и поглощения? Как они возникают? 35. Линейчатый спектр. Как он образуется? 36. Что такое полосатый спектр? Как он образуется? 37. Какой спектр называется сплошным и как он возникает? 38. Пользуясь моделью Бора, укажите спектральные линии, которые могут возникнуть при переходе атома водорода в состояния с 39. Нанесите на шкалу длин волн три линии каждой из двух спектральных серий атома водорода. 40. Что называется спектральной серией? 41. Почему из различных серий спектральных линий атома водорода первой была изучена серия Бальмера? 42. Какой смысл имеют числа 43. Чему равна частота излучения атома водорода, соответствующая коротковолновой границе серии Брэкета? 44. Почему спектр поглощения атома водорода содержит только серию Лаймана? 45. Почему квантовая механика является статистической теорией? 46. В чем отличие понимания причинности в классической и квантовой механике? 1.5. Примерные варианты контроля знаний по модулю I. Вариант 1 1. Электрон движется по окружности радиусом 0,5 см в однородном магнитном поле с индукцией 8 мТл. Определить длину волны де Бройля для электрона. 2. Какую энергию необходимо дополнительно сообщить электрону, чтобы его дебройлевская длина волны уменьшилась от 0,1 нм до 0,05 нм? 3. Частица в бесконечно глубоком, одномерном, прямоугольном потенциальном ящике шириной 4. Какие спектральные линии появятся при возбуждении атомарного водорода электронами с энергией 12,5 эВ? 5. Какую наименьшую энергию нужно сообщить электрону, находящемуся на первой орбите в атоме водорода, чтобы электрон удалился в бесконечность. Вариант 2 1. Вычислить длину волны де Бройля для электрона в кинескопе, ускоряющая разность потенциалов которого 10кВ. надо ли учитывать волновые свойства электрона, если диаметр электронного пучка 1 мм. 2. Оценить с помощью соотношения неопределенностей минимальную кинетическую энергию электрона, движущегося внутри сферической области диаметром 10 нм. 3. Электрон находится в бесконечно глубоком, одномерном, прямоугольном потенциальном ящике шириной 4. Найти наибольшую длину волны в видимой области спектра излучения атома водорода. 5. Какая частота электромагнитной волны, излучаемой атомом водорода, при переходе электрона с четвертого энергетического уровня на третий? Вариант 3 1. Вычислить длину волны де Бройля для пучка протонов, имеющих скорость 103м/с. надо ли учитывать волновые свойства, если диаметр пучка 1мм? 2. Оценить неопределенность импульса протона в ядре. Размер ядра 10-15м. 3. В одномерном потенциальном ящике шириной 4. В каких пределах должны лежать длины волн 5. Заполненный электронный слой характеризуется квантовым числом Вариант 4 1. Пучок альфа-частиц диаметром 1 см прошёл разность потенциалов 100В. надо ли учитывать волновые свойства альфа-частиц при распространении этого пучка? 2. Электрон движется в атоме водорода по первой боровской орбите. Принимая, что допускаемая неопределенность скорости составляет 10% от её значения, определить неопределенность координаты электрона. 3. Вычислить для основного состояния атома водорода радиус круговой орбиты электрона и его скорость. 4. В каких пределах должны лежать длины волн 5. Найти число Вариант 5 1. Надо ли учитывать волновые свойства электронов в атоме водорода? Потенциал ионизации атома водорода 13,6 В, а размер атома порядка 0,53 10-10м. 2. Используя соотношение неопределенностей 3. Электрон находится в потенциальном ящике шириной 4. В каких пределах должна лежать энергия бомбардирующих электронов, чтобы при возбуждении атомов водорода ударами этих электронов спектр водорода имел только одну спектральную линию? 5. Найти наибольшую длину волны в видимой области спектра излучения атома водорода. Вариант 6 1. Вычислить дебройлевские длины волн электрона, протона и атома урана, имеющих одинаковую кинетическую энергию 100эВ. 2. Если допустить, что неопределенность координаты движущейся частицы равна дебройлевской длине волны, то какова будет относительная неопределенность импульса этой частицы? 3. Частица в потенциальном ящике находится в основном состоянии. Какова вероятность 4. При переходе электрона в атоме водорода с одной орбиты на другую, более близкую к ядру, энергия атома уменьшилась на 1,892 эВ. Определить длину волны излучения. |
|

 волновая функция;
волновая функция;  полная энергия частицы;
полная энергия частицы; 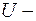 потенциальная энергия частицы (являющаяся функцией координат).
потенциальная энергия частицы (являющаяся функцией координат).

 зарядовое число;
зарядовое число;  элементарный заряд;
элементарный заряд;  электрическая постоянная.
электрическая постоянная.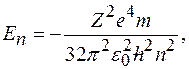
 постоянная Планка;
постоянная Планка;  главное квантовое число
главное квантовое число  .
. функции, описывающей состояние электрона в атоме водорода,
функции, описывающей состояние электрона в атоме водорода,
 квантовые числа: главное, орбитальное, магнитное.
квантовые числа: главное, орбитальное, магнитное. того, что электрон находится в области, ограниченной элементом объема
того, что электрон находится в области, ограниченной элементом объема  , взятого в окрестности точки с координатами
, взятого в окрестности точки с координатами 

 в сферических координатах.
в сферических координатах. состоянии
состоянии  волновая функция сферически-симметричная, т.е. не зависит от углов
волновая функция сферически-симметричная, т.е. не зависит от углов  и
и 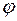 .
. и
и 
 и
и 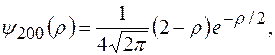

 будет выражаться в безразмерных единицах длины, называемых атомными единицами.
будет выражаться в безразмерных единицах длины, называемых атомными единицами. одинакова по всем направлениям и определяется формулой
одинакова по всем направлениям и определяется формулой
 ,
, орбитальное квантовое число, которое может принимать значения 0, 1, 2, …,
орбитальное квантовое число, которое может принимать значения 0, 1, 2, …,  ;
;  магнетон Бора.
магнетон Бора. ):
):
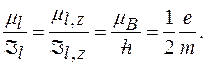
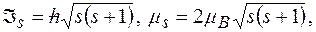
 .
.
 спиновое магнитное квантовое число
спиновое магнитное квантовое число 


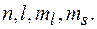
 где
где  внутреннее квантовое число
внутреннее квантовое число 
 где
где  полное орбитальное квантовое число.
полное орбитальное квантовое число.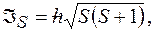 где
где  полное спиновое квантовое число.
полное спиновое квантовое число. где
где  полное внутреннее квантовое число.
полное внутреннее квантовое число. где
где  мультиплетность. Вместо полного орбитального квантового числа
мультиплетность. Вместо полного орбитального квантового числа  пишут символ в соответствии с таблицей:
пишут символ в соответствии с таблицей:

 :
:


 а при
а при  переходы
переходы 

 масса электрона,
масса электрона,  его скорость по
его скорость по 
 постоянная Планка.
постоянная Планка.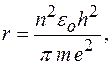
 заряд электрона;
заряд электрона;  электрическая постоянная.
электрическая постоянная.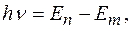
 и
и  соответственно энергии стационарных состояний атома до и после излучения (поглощения).
соответственно энергии стационарных состояний атома до и после излучения (поглощения).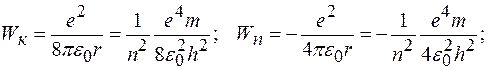


 масса электрона;
масса электрона;  радиус орбиты;
радиус орбиты;  скорость электрона на орбите;
скорость электрона на орбите; 
 или частоту
или частоту  света, излучаемого или поглощаемого атомом водорода при переходе из одного стационарного состояния в другое:
света, излучаемого или поглощаемого атомом водорода при переходе из одного стационарного состояния в другое:

 и
и  постоянная Ридберга,
постоянная Ридберга,  и
и  целые числа;
целые числа;  номер серии спектральных линий (
номер серии спектральных линий (  серия Лаймана,
серия Лаймана,  серия Бальмера,
серия Бальмера,  серия Пашена и т.д.);
серия Пашена и т.д.);  частота излучения. Для данной серии
частота излучения. Для данной серии  и т.д.
и т.д.
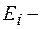 энергия ионизации водорода:
энергия ионизации водорода: 
 электронной орбиты и скорость электрона
электронной орбиты и скорость электрона  на ней связаны равенством:
на ней связаны равенством:
 =1, тогда равенство примет вид:
=1, тогда равенство примет вид:
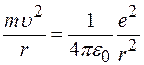 или
или 

 и произведя вычисления, получим:
и произведя вычисления, получим: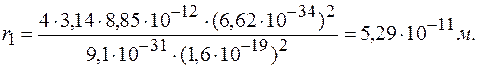

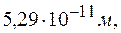




 откуда
откуда

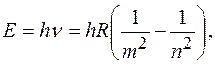


 (1)
(1)
 под действием кулоновской силы:
под действием кулоновской силы: (2)
(2)
 получим с учётом соотношения (2) для радиуса
получим с учётом соотношения (2) для радиуса 


 на орбиту
на орбиту 


 ,
, энергия фотона;
энергия фотона;  постоянная Планка;
постоянная Планка;  скорость света в вакууме;
скорость света в вакууме; 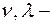 частота и длина волны, соответствующие фотону с энергией
частота и длина волны, соответствующие фотону с энергией 
 ,
, номер энергетического уровня, с которого уходит электрон.
номер энергетического уровня, с которого уходит электрон.


 3 и
3 и  , потенциальную
, потенциальную 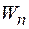 и полную
и полную  энергии электрона на первой боровской орбите.
энергии электрона на первой боровской орбите. и наибольшую
и наибольшую  длины волн спектральных линий водорода в видимой области спектра.
длины волн спектральных линий водорода в видимой области спектра. должны иметь электроны, чтобы при возбуждении атомов водорода ударами электронов появилась эта линия?
должны иметь электроны, чтобы при возбуждении атомов водорода ударами электронов появилась эта линия? (в электронвольтах) должны иметь электроны, чтобы при возбуждении атомов водорода ударами этих электронов появились все линии всех серий спектра водорода? Какую наименьшую скорость
(в электронвольтах) должны иметь электроны, чтобы при возбуждении атомов водорода ударами этих электронов появились все линии всех серий спектра водорода? Какую наименьшую скорость 
 электрона увеличился в 9 раз?
электрона увеличился в 9 раз? 2 и
2 и  переход).
переход). состоянии. Определить: 1) момент импульса (орбитальный)
состоянии. Определить: 1) момент импульса (орбитальный)  электрона; 2) максимальное значение проекии момента импульса
электрона; 2) максимальное значение проекии момента импульса  на направление внешнего магнитного поля.
на направление внешнего магнитного поля. и
и  можно говорить о движении частицы по определенной траектории?
можно говорить о движении частицы по определенной траектории? частицы, движущейся со скоростью 107 м/с, если ее положение оценивается по ширине следа в камере Вильсона (10-4м)?
частицы, движущейся со скоростью 107 м/с, если ее положение оценивается по ширине следа в камере Вильсона (10-4м)? Найти решение уравнения.
Найти решение уравнения.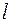 находится в возбужденном состоянии с
находится в возбужденном состоянии с  , равноудаленном от стенок ящика.
, равноудаленном от стенок ящика. электронов в этом слое, которые имеют одинаковые квантовые числа: 1)
электронов в этом слое, которые имеют одинаковые квантовые числа: 1)  2)
2)  2.
2. и
и  слои,
слои,  оболочка и наполовину
оболочка и наполовину 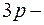 оболочка.
оболочка. найти выражение, позволяющее оценить минимальную энергию
найти выражение, позволяющее оценить минимальную энергию 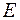 электрона, находящегося в одномерном потенциальном ящике шириной
электрона, находящегося в одномерном потенциальном ящике шириной 
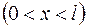 плотность вероятности нахождения электрона на первом и втором энергетических уровнях одинакова?
плотность вероятности нахождения электрона на первом и втором энергетических уровнях одинакова?