|
|
Где Э – эквивалент определяемого иона.
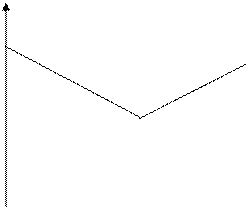
L, Ом-1
V1 Объем раствора реагента Рис.4.24. Кривая кондуктометрического титрования.
ЗАДАНИЕ 6. Методика определения рН и буферной емкости Почвенных растворов 1. Получение почвенной вытяжки. 10 г почвы заливают 50 см3 дистиллированной воды и встряхивают на качалке в течение 10-15 мин. Смесь фильтруют через предварительно смоченный складчатый фильтр, а фильтраты используют для определения рН и буферной емкости. Для определения общей кислотности навески почвы заливают 50 см3 0,1н KCl или NH4Cl и проводят только потенциометрическое определение рН.
2. Колориметрическое определение проводят путем сравнения окраски капли фильтрата на полоске универсальной бумаги с цветной шкалой индикатора; или 5-7 см3 почвенной вытяжки помещают в пробирку и добавляют 2-3 капли раствора универсального индикатора. Затем сравнивают цвет почвенной вытяжки с окраской стандартных растворов в наборе Алямовского. Записывают значение рНкол = …
3.Потенциометрическое определение рН проводят с помощью потенциометра (иономера), (см. инструкцию). Данные записывают в табл. 4.17.
Таблица 4.17. Результаты потенциометрических измерений
4.Определение буферной емкости. В два стаканчика отмеряют по 10 см3 почвенной вытяжки. В один добавляют 1 см3 0,1 н NaOH, в другой 1 см3 0,1 н HCl. Измеряют рН, данные записывают в таблицу 12. По уравнениям (4.162) и (4.81) вычисляют буферную емкость почвенного раствора. Делают выводы.
ЗАДАНИЕ 7. Методика выполнения работы по изучению свойств буферных растворов Опыт 1.Влияние разбавления на свойства буферной смеси
В плоскодонной колбе готовят смесь, отбирая из бюретки: 6 см3 0,1 н СН3СООН или NH4OH 14 см3 0,1 н СН3СООNa или NH4Cl Измеряют рН приготовленной смеси и разделяют ее на две равные части (по 10 см3). К одной из частей прибавляют 10 см3, а к другой 20 см3 дистиллированной воды. После тщательного перемешивания растворов измеряют их рН, данные заносят в табл. 4.17.
Таблица 4.17. Влияние разбавления на рН буферной смеси
Делают вывод о влиянии разбавления на рН буферных растворов.
Опыт 2. Изучение действия кислот и щелочей на величину рН буферного раствора В колбе аналогично опыту 1 готовят буферную смесь состава: 6 см3 0,1 н СН3СООН или NH4OH 14 см3 0,1 н СН3СООNa или NH4Cl Измеряют рН приготовленной смеси, разделяют ее на две равные части . К одной из них прибавляют 1 см3 0,1 н HCl; к другой – 1 см3 0,1 н NaOH. Измеряют рН полученных растворов, для контроля аналогичные действия выполняют с дистиллированной водой. Все данные заносят в табл. 4.18
Таблица 4 .18 Буферное действие смесей
Делают вывод о буферном действии.
Опыт 3. Изучение зависимости рН и буферной емкости от соотношения концентрации компонентов смеси
Готовят буферные смеси согласно указанных в табл. 4.19 соотношений.
Таблица 4.19. Зависимость рН и буферной емкости от соотношения концентрации компонентов
Измеряют рН приготовленных смесей. Затем, разделив на две части, к одной части прибавляют 1 см3 0,1 н HCl, к другой – 1 см3 0,1 н NaOH. Измеряют рН всех растворов и записывают в табл. 15. Рассчитывают по формулам (4.162) и (4.81) значения буферной емкости отдельно по кислоте и щелочи. Отмечают в выводах, при каком соотношении компонентов буферной смеси буферная емкость наибольшая, соответствуют ли ваши опытные данные теории буферных систем.
ЗАДАНИЕ 8. Потенциометрическое определение рН и расчет активности водородных ионов в буферных растворах В 5 пробирок отмеряют из бюреток 0,1 н раствора СН3СООН (NH4OH) и СН3СООNa (NH4Cl) в соотношении, указанном в таблице 4.20 Таблица 4.20
Зная, что рН = -lgaH+, рассчитывают активность водородных ионов. Данные заносят в таблицу 4.20. Расчет величины рН при равных концентрациях компонентов осуществляют по уравнениям: для кислых буферных систем pH = рКд + lgVc – lgVк , (4.164)
для основных буферных систем pH = pKв –рКд + lgVо – lgVс, (4.165)
где: Кд – константа слабой кислоты или основания (см. приложение, табл. 5); Кв – ионное произведение воды (см. Приложение); Vк, Vо, Vс - объемы соответственно взятых кислот, основания или соли. Данные заносят в таблицу, после чего получают контрольный раствор, измеряют его рН и рассчитывают ан , а также объемы взятых компонентов. Проводят расчет ошибки опыта. Делают выводы.
СОДЕРЖАНИЕ Введение 3 ПРАВИЛА РАБОТЫ В ЛАБОРАТОРИЯХ ФИЗИЧЕСКОЙ И КОЛЛОИДНОЙХИМИИ 10 Математические понятия 11 Тема1 |
|