|
|
Электролитпен коагуляциялау кинетикасы 9 главаАЛҒЫ СӨЗ «Қазақ университеті» баспасынан аз тиражбен 2002 жылы шыққан «Коллоидтық жүйелердің жалпы қасиеттері» атты оқу құралымыз бүгінде библиографиялық тапшылыққа айналды. Коллоидтық химиядан жазылып жатқан оқулықтың жарық көруіне әлі біраз уақыттың кететінін және қазіргі таңда университеттердің химия факультеттерінде қазақ бөлімінде оқитын студенттердің сұранысын еске ала отырып, бұрынғы оқу құралын өңдеп, толықтырып әзірге студенттер кәдесіне жаратуды жөн көрдік. Бұрынғы оқу құралына «Коллоидтық химия нысандарының басты белгілері; Коллоидтық (дисперстік) жүйелердің классификациясы; Опалесценция мен флуоресценцияның айырмашылығы; Зерттеудің электронграфтық және рентгенграфтық әдістері; Седиментациялық талдау әдістемесі; Электркапиллярлық құбылыстар» сияқты жаңа тақырыптар қосылды және бұрынғы тақырыптардың біразы толықтырылды. Оқу құралында коллоидтық жүйелердің барлық қасиеттері емес, тек оптикалық, молекулалы-кинетикалық және электрлік қасиеттері ғана қарастырылғандықтан оны «Коллоидтық жүйелердің молекулалы-кинетикалық, оптикалық және электрлік қасиеттері» деп атадық. Жаңа оқу құралы студенттер мен оқытушылардың қажеттілігін өтеп, қазақ бөлімінде оқитын студенттердің білім дәрежесін арттыруға себебін тигізетініне сенімдіміз.
автор: Ә.Қоқанбаев әл-Фараби атындағы ҚазҰУ-нің профессоры БІРІНШІ ТАРАУ КІРІСПЕ 1.1 Коллоидтық химияның дамуына қысқаша тарихи шолу Коллоидтық химия алғашқы кезде физикалық химияның бір тарауы ғана болатын. Ол физикалық химия сияқты физика мен химияның аралық облысын зерттейді. ХХ-ғасырдың бастапқы кезіне дейін коллоидтық химия негізінен алғанда тек жоғарғы дисперстік жүйелер қасиеттері мен коллоидтық ерітінділерді даярлау тәсілдерін зерттеді. Бертін келе коллоидтық жүйелер мен коллоидты – химиялық үдерістердің зор мәніне байланысты, оның үстіне теория мен практикалық мәліметтердің көбеюіне байланысты коллоидтық химия жеке ғылыми пән болып қалыптасты. Қазіргі кезде коллоидтық химияның өзіне тән зерттеу әдістерінің тек химия үшін емес басқа да биология, геология, медицина, топырақ зерттеу т.б. ғылымдар үшін маңызы зор. Атап айтқанда олар: ультрамикроскоптық, электрондық микроскоптық, ультрацентрифугалық, электрофорездік, нефелометрлік, вискозиметрлік, осмометрлік және т.б. әдістер. Қазіргі кезде коллоидтық жүйелер мен коллоидты-химиялық үдерістердің және олардың зерттеу тәсілдерінің қолданбайтын халық шаруашылығының салаларын атап айту қиынға соғады. Міне, осы айтқанның бәрі коллоидтық химияның жеке ғылым болуына әсерін тигізді. Коллоидтық химия нені зерттейтінін ақиқат білу үшін алдымен оның дамуына қысқаша шолу жасап, сосын «Коллоид» дегеніміз не? «Колоидтық жүйе» дегеніміз не? деген сұрақтарға жауап беруге тура келеді. Адам баласы коллоидтық жүйелермен өте ерте кезден-ақ таныс болып, олардың өз керегіне қолдана бастаған. Ертеде Қытай, Үнді, Мысыр, Грек, Рим халықтары тамақ даярлау, тері илеу, мата бояу, т.б. үшін коллоидтық құбылыстарды қолданған болатын. 1852 жылы М.В. Ломоносов коллоидтық ерітінділерді зерттей отырып, сол кездің өзінде-ақ жаңа өндірістің негізін салды. Ол-түсті шыны өндірісі еді. Бұл үшін М.В. Ломоносов алтынның коллоидтық ерітіндісін (алтынның зольін) қолданған болатын. Ең бірінші ерітінділердің қатты дененің бетіндегі – адсорбенттердегі адсорбциясын 1792 жылы орыс химигі Ловиц зерттеген болатын. Ол қатты адсорбент – көмір арқылы ерітінділерді тазартты. 1808 жылы Мәскеу университетінің профессоры Рейсс коллоидтық ерітінділердің электрлік қасиеттерін байқап, электрофорез, электросмос құбылыстарын ашты. Ол бұл құбылыстарды топырақ жүзгіндерін (суспензияларын) тексеру арқылы ашты. 1845 жылдан бастап италян ғалымы Франциско Сельми коллоидтық жүйелерді зерттей бастады. Ол хлорды күміс, күкірт, берлиндік лазурьдің судағы ерітінділерінен тұратын жүйелерді зерттеді. Бұл заттардың суда ерімейтіні белгілі бола тұрса да, Сельми алған жүйелер сырт жағынан қарағанда мөлдір кәдімгі (шын) ерітінділерге ұқсас болды. Сельми осы заттардың судағы NaCl, CuSO4 cияқты тұздардың ерігендегі мөлшеріндей ұсақ бөлшектер сияқты емес екенін атап көрсетті. Бұндай ерітінділерді кәдімгі ерітінділерден айыру үшін Сельми оларды псевдо (жалған) ерітінділер деп атады. Швед ғалымы И.Я. Берцелиус 1824-1934 жылдардағы еңбектерінде жуу кезінде сүзгіден өтіп кететін біраз тұнбалардың қасиеттерін жазған болатын. Мысалы, кремний және ванадий қышқылдарының тұнбалары, күкіртті темір,хлорлы күміс, берлиндік лазурь және т.б. оларды сумен жуғанда қайтадан ерітіндіге айналатынын және олардың қасиеттері кәдімгі ерітіндіден өзгеше болатынын көрсетті. Бұл ерітінділердің қасиеттері жүзгіндер (суспензиялар) мен майғындар (эмульсиялардың) қасиеттеріне жақын екенін көрсетеді. Аналитикалық химиядағы сүзгіден өткен тұнбаларды таза сумен емес, оларға сәйкес электролиттің ерітіндісімен жуу туралы ережені Берцелиус айтқан болатын. Осы қарастырып отырған ерітінділер – қазіргі түсінік бойынша коллоидтық жүйелер. Псевдоерітінділердің өзіне тән мынандай қасиеттері болды. Олар сәулені өте күшті шашыратады, осы заттарға әсер етпейтін тұздарды ерітіндігі өте аз мөлшерде қоссақ та олар тұнбаға түседі. Ф.Сельмидің түсінігіндей түсінік К. Нэгелиде де болды. Ол хлорлы күміс, күкірт бөлшектері т.б. заттардың жоғарғыда айтқандай жүйелерде олардың кәдімгі молекулаларға қарағанда үлкенірек агрегат күйінде болатынын айтты. Осы сияқты көп молекулалы агрегаттарға К. Нэгели «мицелла» деген ат берді. Ал кірне мицелла болатын жүйені «золь» (кірне) деп атады. Осы атаулар коллоидтық химияда қазіргі кезде де қолданылады. 1857 жылы М.Фарадей құрамында алтыны бар су көлемінде бөлінген жүйелердің (ондай жүйелер бұрынырақ алхимиктерге белгілі болатын) оптикалық қасиеттерін тексеріп, алтын осы жүйелерде өте кішкентай бөлшек күйінде болады деген қорытындыға келді. 1861 жылы ағылшын ғалымы Т. Грэм жасаған зерттеулер коллоидтық химияның дамуында үлкен роль атқарды. Ол барлық заттарды диффузия жылдамдығы бойынша екі класқа бөлді: жақсы диффузияаланатын заттар (кристаллоидтар) және нашар диффузияланатын заттар (коллоидтар). 1 – ші топқа әртүрлі электролиттер жатса, II – ші топқа Грэм крахмал, белок, агар-агар т.б. физикалық жағынан желімге ұқсас затарды жатқызды. «Колла»- латынша желім деген сөз. Мысалы ол электролиттер мен аталған заттаарды салыстыра отырып, мынаны байқайды. Тұз қышқылы жұмыртқа (тұқым) белогіне қарағанда 50 рет, крахмалға қарағанда 100 рет артық диффузияланады. Грэм коллоидтарды кристалдардан бөлетін «диализ» деген тәсіл жасады. Ол үшін Грэм табиғи, иә жасанды материалдар алынған кристалдарды өз бойынан өткізіп жіберетін, ал коллоидтарды ұстап қалатын қасиеттері бар пленкалар (қабыршықтар) қолданды. Заттарды екі топқа бөле отырып, Грэм кристалды заттар золь түзбейді деген ұғымда болды. Бұған қарама-қарсы, Грэмнің замандасы Киевтің профессоры И.Б. Борщев 1869 жылы коллоидтық жүйелердің кристалдық құрылысы болуы да мүмкін деген жорамал айтты. Оның «Өсімдік пен жануарлардың организмдерінің түзілуіне қатысатын коллоидтардың қасиеттері мен құрылысы» деген классикалық еңбегін атап көрсеткен жөн. Бұл еңбегінде И.Б.Борщев коллоид туралы түсінігін тұжырымдады. Коллоидтық жүйені ол көп фазалық (гетерогендік) жүйе деп атап көрсетеді (бір фазалық шынайы негайы негзгі ерітіндіден айырмашылығы ). ХХ – ғасырдың бастапқы кезінде Борщевтің айтқанын орыс ғалымы Веймарн эксперимент бойынша дәлелдеді. Ол 200 – ден астам жәй жағдайда кристалдық күйде болатын заттарды коллоидтық күйінде де алды. Сөйтіп, бір заттың жағдайға байланысты кристалдық та және коллоидтық та қасиет көрсететіні дәлелденді. Мысалы, ас тұзы суда шын ерітінді, бензолда-коллоидтық ерітінді түзсе, шайыр спиртте ерігенде шын ерітінді, ол суда коллоидтық ерітінді түзеді. Міне осы айтылған жұмыстар жалпыға бірдей қабылданып, Грэмнің түсініктерінің дұрыс емес екені ақиқатталды. Сонымен коллоидтық зат емес, заттың коллоидтық күйі деп айтуымыз дұрыс болады. 1871 жылы өзінің «Основы химии» («Химия негіздері») деген еңбегінде Д.В. Менделеев Грэмнің жұмыстарына үлкен мән берді. Заттың коллоидтық күйі (коллоидтық жүйе) – заттың бөлшектері жеке молекула емес, молекулалардың біріккен түрі – агрегаттардан тұратындығын, көптеген ізденістердің нәтижесінде дәлелденді. Осыны біле отырып, заттың коллоидтық күйінің (коллоидтық жүйенің) жәй ерітінділерден ерекшелігін түсіндіруге болады. Коллоидтық бөлшек бірнеше молекулалардан тұратын болғандықтан оларға фазалардың термодинамикалық қасиеттерін қолдануға болады, ал осы коллоидтық бөлшектерді диспергілеп (ұнтақтап, ұсақтап) тұрған орта басқа фаза түзеді. Осыдан кез келген коллоидтық ерітінді – гетерогендік жүйе, яғни көп фазалық, ең қарпайым күйінде – қос фазалық жүйе. Бұл-олардың бір фазалы болып келетін шын ерітінділерден айырмашылығының бірі. Коллоидтық ерітінді гетерогендік жүйе болғандықтан оның түзілуі үшін бір фазадағы заттың екінші фазадағы затта ерімеуі керек, иә өте нашар еруі керек. Тек осы жағдайда ғана заттар арасында шектелген бөлінген бет пайда болады. Осыған байланысты коллоидтық ерітінді ең кемі екі, иә көп құрамдасты жүйе болады. Осы жоғарғы айтылғандардан коллоидтық жүйе деп бір дененің (дисперстік фаза) басқа бір денеде (дисперсиялық дисперстеуші ортада) диспергіленген (ұнтақталған, ұсақталған, майдаланған,шашыраған) күйін айтамыз. Осыған байланысты коллоидтық химияны гетерогендік жоғарғы дисперстік жүйелердің қасиеттері мен онда жүретін үдерістерді зерттейтін ғылым деп айтуға болады. Біз өткен ғасырдағы жиналған фактілерге сүйене отырып, коллоидтық химияға осындай анықтама беріп отырмыз. Алайда ХХ – ғасырдың басынан бастап коллоидтық химия теориялық жағынан одан әрі дамыды. Мысалы, Смолуховский (1906 ж) және Эйнштейн (1908 ж) броундық қозғалыс пен коллоидтық жүйедегі диффузияның теориясын жасады, Перрен, Сведберг, Ильин, айталған теорияны эксперимент арқылы растап берді. ХІХ – ғасырдың аяғы мен ХХ – ғасырдың басында химиктерді ойландырған мәселелердің бірі – ерітінділердің табиғаты еді. Әрине мұнда коллоидтық ерітінділер туралы да сөз болып отыр. Ол кезде коллоидтық ерітінділердің табиғаты туралы, оның кәдімгі ерітінділерден принциптік айырмашылығы бола ма деген мәселелер маңында ұзақ пікірталастар болды. Бұған жауап ретінде негізгі екі бағыт пайда болды. Бірі – суспензиялық (жүзгіндік) оны Барус, Шнайдер т.б. қолдаса, екіншісі – ерітінділік теория (Линдер, Пиксон және т.б.). Екінші бағытты қолдаған Зигмонди өзінің көзқарасын өзі кейінірек теріске шығарды. 1903 ж Ф. Зигмонди, Г. Зидентопфпен бірігіп ультрамикроскоп деген құрал жасады, ол коллоидтық химияның жылдам дамуына әсерін тигізді. Коллоидтық химияның дамуында үлкен көп роль атқаратын физика мен физикалық химияның ХІХ – ғасырдың аяғы мен ХХ – басында орындалған көптеген фундаменталдық (іргелі) зерттеулерді айта кеткен жөн. Олар: П. Лапластың (1805 ж.) капиллярлық теориясы (В. Гиббстің 1887 ж. фазалар ережесі, беттік құбылыстың теориясы), Ж. Рэлейдің 1871 ж., Шульце (1882 ж) мен Гардидің 1900 ж. коллоидтардың коагуляциясы, И. Лэнгмюрдің (1917 ж. адсорбция теориясы мен мономолекулалық беттік қабаттың құрылысы), А.В. Думанскийдің (1903 ж. коллоидтық ерітінділердің электрөткізгіштігі, 1918 ж. центруфуганы коллоидтық бөлшектердің шамасын, мөлшерін анықтау үшін қолдануы), М.С. Цветтің (1903 ж. хромотография ашуы, Л.Г. Гурвичтің (1912-1917 ж. беттік құбылыстарды тексеруі), Антонов (1907 ж. ерітінділердің беттік керілуі) пен Шишковскийдің (1908 ж.) және т.б. ғалымдардың еңбектері. Бұл зертеулермен коллоидтық химияның толық курсын оқу арқылы таныса жатамыз. Бұрын Одақ көлемінде коллоидтық химия Ұлы Қазан революциясынан кейін одан әрі кең өріс алып дами бастады. Бір қатар ғылыми-зерттеу институттардың ашылуы кеңес ғалымдарының творчестволық еңбектерінің жемісті болуына мүмкіншілік берді. Н.П. Песков (1917 ж.) коллоидтық жүйенің агрегативтік және седиментациялық тұрақтылығы жөніндегі ілімнің негізін салды. Коллоидтық жүйелердің тұрақтылығы мен коагуляциясын зерттеуде Фрейндлих, Кройт, Рабинович, Дерягин т.б. ғалымдардың еңбектерінің үлкен маңызы бар. Ребиндер және оның шәкерттерінің адсорбциялық қабаттың коллоидтық жүйелердің қасиетіне әсерін және олардың құрылымдық-механикалық қасиеттерін зерттеулері коллоидтық химияның дамуында үлкен орын алды. Осы зерттеулердің нәтижесінде коллоидтық жүйелердің қасиеттерін меңгеретін әдіс ашылды. Олар Кеңес Одағының өнеркәсібінің көптеген салаларында қолдана бастады. Қызықты бір жәйт-коллоидтық химияның дамуында коллоидтық емес жүйелерді зерттеу де үлкен орын алды. Жоғарғы молекулалық қосылыстарды басқаша, айтқанда полимерлер деп аталатын класты біз білеміз. Оларға белок, каучук, целлюлоза т.б. жасанды заттар жатады. Осы заттардың ерітінділерін зерттеудің арқасында олардың шын ерітінді екені дәлелденді. Сонысына қарамастан олар коллоидтық жүйелердің қасиеттеріндей қасиет көрсетіні байқалды. Сондықтан жоғарғы молекулалы қосылыстардың ерітінділері гомогендік жүйе бола тұра коллоидтық химия курсында қарастырылады. Осыған байланысты коллоидтық химияға мынандай анықтама беруге болады. Беттік құбылыстарға сүйене отырып жоғары дисперстік гетерогендік жүйелер мен жоғары молекулалық қосылыстардың және олардың ерітінділердің физикалық-химиялық қасиеттерін зерттейтін химиялық пәнді колоидтық химия дейміз. Коллоидтық жүйелер мен жоғарғы молекулалы ерітінділердің қасиеттерін зерттеуде Н.П. Песков, И.И. Жуков, А.В. Думанский, В.А. Каргин, Б.В. Дерягин, Б.А. Догадкин, С.С. Воюцкий, А.И. Рабинович т.б. ғалымдардың еңбектерінің маңызы зор. Коллоидтық химияның жалпы курсын оқу арқылы, келесі тарауларда жоғарғы да айтылған зерттеулермен толығырақ танысамыз.
1.2 Заттың коллоидтық күйінің негізгі ерекшеліктері Заттың коллоидтық күйінің негізгі ерекшеліктерінің бірін біз жоғарыда айтып өттік. Ол - коллоидтық күйдің жүйенің гетерогенділігі, яғни екі иә одан да көп фазадан тұратындығы. Мұндағы фазалардың бірі өте ұсақ бөлшектерден (дисперстік фаза) тұрса, екіншісі сол бөлшектерді ұсақтаушы орта – дисперстеуші ортадан тұруы. Енді сол дисперстік фазаның шамасын (өлшемін) көрсететін-дисперстілік деген ұғымға тоқталайық. Кез келген дисперстік жүйеде иә бөлшектердің көлденең қимасының ұзындығын а, (егер бөлшек шар тәрізді болса диаметрі d, егер бөлшек куб сияқты болса, кубтың қабырғасы-1), иә оған кері шаманы D=1/а қарастыруға болады. Әр түрлі оқулықтарда дисперстілік бірлігін әртүрлі өлшемдермен көрсетеді. Олардың арасында байланыс былайша болады (1-кестені қара).
1-кесте
Бұнда D-ні әдетте дисперстілік деп айтады. Ол сол бөлшектердің меншікті бетінің ауданына пропорционалдық шама, яғни бөлшектің шамасы кеміген сайын дисперстілік пен меншікті беттің ауданы өседі де, керісінше бөлшектің шамасы өскен сайын кейінгі шамалар кемиді. Беттік ауданның дисперстік фазаның бөлшектеріне мөлшеріне байланысты тәуелділігінің өзгеруін куб тәрізді бөлшекті мысалға ала отырып көрсетуге болады. (2-кестені қара).
2-кесте
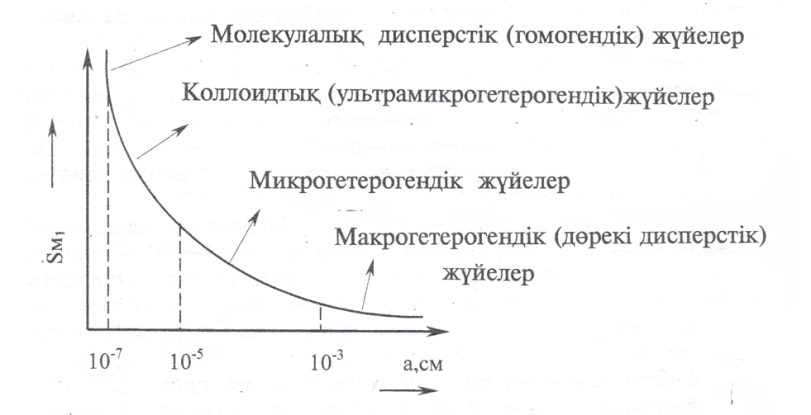
Коллоидтық жүйеге, a-ның мәні 10-7÷10-5 см болатын жүйелер жатады. Коллоидтық жүйенің дисперстілігінің жоғарғы шегінің болуы бөлшектерді одан әрі бөлінгенде олардың агрегат емес жеке молекулалар күйінде болуы, ал оның төменгі шегі бөлшектердің шамасы а=10-5 см болғанда қозғалысының қарқынының өте азаюымен анықталады. 2 – кестедегі мәліметтер бойынша мынаны байқауға болады. Тек гетерогендік жоғарғы дисперстік коллоидтық бөлшектер ғана ең күшті дамыған меншікті беттер түзеді. Осыған байланысты коллоидтық жүйе дисперстік жүйелердің ішінде ерекше орын алады. Бөлшектер шамасының дөрекі дисперстік жүйеден молекулалық дәрежедегі жүйеге өзгеруіне байланысты олардың меншікті беттері 1.1- суреттегі көрсетілген диаграмма бойынша өзгеретінін байқауға болады.
Сурет Дөрекідисперстік жүйенің молекулалы – дисперстік жүйеге көшуі үзіліссіз болғанымен микрогетерогендік жүйе мен коллоидтық жүйенің жағдайлары өздерінше ерекше. Меншікті беттерінің үлкендігіне (көптігіне) байланысты оларда адсорбция, жалпы беттік құбылыстар күшті болады. Ол жөнінде курстың лайықты тарауларында толығырақ танысамыз. Коллоидтың жүйелердің тағы бір ерекшелігі-олардың агрегаттық тұрақсыздығы. Оның себебін термодинамикалық және кинетикалық тұрғыдан түсіндіруге болады. Коллоидтық жүйелердің меншікті беттері үлкен болғандықтан оған лайық еркін беттік энергиялары да артық болады. Ал артық еркін беттік энергиясы болатын жүйе әрқашанда тұрақсыз, олар сол энергияны азайтуға тырысады. Осыған байланысты коагуляцияланады (тұнбаға түседі). Коллоидтық тұрғыдан қарағанда коллоидтық жүйенің тұрақтылығы, тұрақсыздығы жүйедегі дисперстік фазаның бөлшектерінің арасындағы күштерге байланысты. Ол күштер: тарту күштері, басқаша айтқанда бөлшектерді жақындататын атракциондық күштер және коагуляцияға кедергі болатынын-тебу күштері. Коллоидтық жүйенің тұрақты, иә тұрақсыз болуы осы күштердің қатынасына байланысты. Коллоидтық жүйелер жарықты шашырататын да қасиет көрсетеді (опалесценция). Бұл құбылысты әсіресе оларға жарықты бір жанынан жарық көзі мен коллоидтық ерітінді аралығында линзалар қойып байқауға болады. Онда біз жарқылдайтын конусты (Тиндаль конусы) көреміз. Бұл коллоидтық ерітіндінің әртектілігін көрсетеді. Коллоидтық ерітінділерде шын ерітінділерге қарағанда диффузия өте жай жүреді. Коллоидтық ерітінділердің осмостық қосымы да өте аз, сондықтан көп жағдайда оны байқау да қиынға соғады. Коллоидтық жүйелердің осы соңғы айтқан екі қасиеті дисперстік фазаның бөлшектерінің ірі екендігін көрсетеді. Осындай ірі бөлшектердің болуына байланыста коллоидтық ерітінділерді диализдеуге болады. Диализ кезінде (Грэмның жұмыстары) кіші молекулалы заттар жарғақтан өтіп кетеді де, ал коллоидтық бөлшектер өтпей қалады. Коллоидтық жүйелер көбіне (бірақ барлық жағдайда емес) электркинетикалық қасиеттер (ол жөнінде арнайы IV – тарауда токталамыз) көрсетеді.Бұл айтылған ерекшеліктер коллоидтық жүйелерге тән болғандықтан, осы курсты оқу барысында оларды бір емес бірнеше рет кездестіріп және олардың жоғарғыда айтылмаған басқа да қасиеттерімен танысамыз. Коллоидтық жүйелерді шын ерітінділер мен дөрекі дисперстік микрогерогендік жүйелермен салыстыра отырып, олардың ерекшелігін мынадай кестемен көрсетуге болады. Коллоидтық жүйелер дисперстілік шамасы жағынан микрогетерогендік жүйелер мен шын ерітінділердің аралығында болғандықтан, кейбір қасиеттері микрогетерогендік жүйелерге, ал кейбір қасиеттері шын ерітінділерге ұқсас екенін байқауға болады (3-ші кестені қара).
3 – кесте.
|
|