|
|
Источник и приемник движутся друг относительно друга.Этот случай обобщает два предыдущих. Частота колебаний, воспринимаемых приемником: Верхний знак берется, если при движении источника или приемника происходит их сближение, нижний знак — в случае их взаимного удаления. Если направления скоростей не совпадают с проходящей через источник и приемник прямой, то вместо этих скоростей в формуле надо брать их проекцию на направление этой прямой.
«Если бы в результате какой-то мировой катастрофы все накопленные научные знания оказались бы уничтоженными и к грядущим поколениям живых существ перешла бы только одна фраза, то какое утверждение, составленное из наименьшего количества слов, принесло бы наибольшую информацию? Я считаю, что это — атомная гипотеза (можете называть её не гипотезой, а фактом, но это ничего не меняет): все тела состоят из атомов — маленьких телец, которые находятся в беспрерывном движении, притягиваются на небольшом расстоянии, но отталкиваются, если одно из них плотнее прижать к другому. В одной этой фразе, как вы увидите, содержится невероятное количество информации о мире, стоит лишь приложить к ней немного воображения и чуть соображения». Ричард Фейнман http://www.i1t.kharkov.ua/bvi/ogurtsov/ogurtsov.htm http://kart.edu.ua/books/ln/index.html
1. Статистический и термодинамический методы исследования. Молекулярная физика и термодинамика — разделы физики, в которых изучаются зависимости свойств тел от их строения, взаимодействия между частицами, из которых состоят тела, и характера движения частиц. Для исследования физических свойств макроскопических систем, связанных с огромным числом содержащихся в них атомов и молекул, применяют двакачественно различных и взаимно дополняющих друг друга метода: статистический (или молекулярно-кинетический) и термодинамический. Статистический метод— это метод исследования систем из большого числа частиц, оперирующий статистическими закономерностями и средними (усредненными) значениями физических величин, характеризующих всю систему. Этот метод лежит в основе молекулярной физики — раздела физики, изучающего строение и свойства вещества исходя из молекулярно-кинетических представлений,основывающихся на том, что все тела состоят из атомов, молекул или ионов находящихся в непрерывном хаотическом движении. В дальнейшем мы будем использовать термин "молекула" имея ввиду мельчайшую структурную единицу (элемент) данного вещества. Термодинамический метод— это метод исследования систем из большого числа частиц, оперирующий величинами, характеризующими систему в целом {например, давление, объем, температура) при различных превращениях энергии, происходящих в системе, не учитывая при этом внутреннего строения изучаемых тел и характера движения отдельных частиц. Этот метод лежит в основе термодинамики — раздела физики, изучающего общие свойства макроскопических систем, находящихся в состоянии термодинамического равновесия, и процессы перехода между этими состояниями. 2. Термодинамическая система. Термодинамика имеет дело с термодинамической системой — совокупностью макроскопических тел, которые взаимодействуют и обмениваются энергией как между собой, так и с другими телами (внешней средой). Термодинамические системы, не обменивающиеся с внешней средой ни энергией, ни веществом, называются замкнутыми. Основа термодинамического метода — определение состояния термодинамической системы. Состояние системы задается термодинамическими параметрами (параметрами состояния) — совокупностью физических величин, характеризующих свойства термодинамической системы. Обычно в качестве параметров состояния выбирают температуру, давление и объем. Параметры состояния системы могут изменяться. Любое изменение в термодинамической системе, связанное с изменением хотя бы одного из ее термодинамических параметров, называется термодинамическим процессом. Если для данной системы внешние условия не изменяются и состояние системы с течением времени не меняется, то этасистема находится в термодинамическом равновесии. 3. Температура. Температура — одно из основных понятий, играющих важнейшую роль в физике в целом. Температура — физическая величина, характеризующая состояние термодинамического равновесия макроскопической системы и определяющая направление теплообмена между телами. В настоящее время используют две температурные шкалы. Международная практическая шкала (шкала Цельсия )градуированная в градусах Цельсия (°С) по двум реперным точкам — температурам замерзания и кипения воды при давлении 1,013∙105 Па, которые принимаются соответственно 0°С и 100°С. Термодинамическая температурная шкала (шкала Кельвина), градуированная в градусах Кельвина (К) определяется по одной реперной точке — тройной точке воды — температуре, при которой лед, вода и насыщенный пар при давлении 609 Па находятся в термодинамическом равновесии. Температура этой точки по данной шкале равна 273,16 К. Температура Т = 0 К называется нулем Кельвина. Термодинамическая температура (Г) и температура (t) по Международной практической шкале связаны соотношением Т = 273,15 +t Нормальные условия: Т0 = 273,15 К = 0°С, р0 = 101325 Па. 4. Идеальный газ. Физическая модель, согласно которой: 1) собственный объем молекул газа пренебрежимо мал по сравнению с объемом сосуда; 2) между молекулами газа отсутствуют силы взаимодействия; 3) столкновения молекул газа между собой и со стенками сосуда абсолютно упругие. Исходя из этого идеальный газ можно рассматривать как совокупность беспорядочно движущихся молекул-шариков, имеющих пренебрежимо малый собственный объем и не взаимодействующих друг с другом на расстоянии. Законы, описывающие поведение идеальных газов — законы Бойля-Мариотта, Авогадро, Дальтона, Гей-Люссака.
Для данной массы газа m при постоянной температуре Т произведение давления р на объем V есть величина постоянная: pV = const при Т = const и m = const Кривая, изображающая зависимость между р и V, характеризующая свойства вещества при постоянной температуре, называется изотермой.Изотермы — гиперболы, расположенные на графике тем выше, чем выше температура происходящего процесса. 6. Закон Авогадро, Количество вещества V— физическая величина, определяемая числом специфических структурных элементов — молекул, атомов или ионов, из которых состоит вещество. Единица количества вещества — моль— количество вещества системы, содержащей столько же структурных элементов, сколько содержится в 0,012 кг изотопа углерода 12С.
Закон Авогадро: моли любых газов при одинаковой температуре и давлении занимают одинаковые объемы.
Молярная масса Единица молярной массы — килограмм на моль (кг/моль). 7. Закон Дальтона. Парциальное давление — давление, которое производил бы газ, входящий в состав газовой смеси, если бы он один занимал объем, равный объему смеси при той же температуре. Закон Дальтона:давление смеси идеальных газов равно сумме парциальных давлений р1,р2,...,рn входящих в нее газов: p =p1+p2+--- + pn или
1) Давление р данной массы m газа при постоянном 2) Объем V данной массы m газа при постоянном Процесс,протекающий при постоянном давлении, называется изобарным. На диаграмме в координатах (V,t) этот процесс изображается прямой, называемой изобарой.
Процесс,протекающий при постоянном объеме, называется изохорным. На диаграмме в координатах (p,t) он изображается прямой, называемой изохорой. Изобары и изохоры пересекают ось температуры в точке шкалу Кельвина (термодинамическую температуру): В термодинамической шкале температур: V = V0(1 + αt) = V0αT, p = p0(1 +αt) = р0αТ Откуда:
где индексы 1 и 2 относятся кпроизвольным состояниям, лежащим на одной изобаре или изохоре. 9. Уравнение состояния идеального газа. Уравнением состояния термодинамической системы называется уравнение, которое связывает давление р, объем V и температуру Т термодинамической системы, находящейся в состоянии термодинамического равновесия: f(p,V,T) = 0 где каждая из переменных является функцией двух других.
Пусть некоторая масса газа занимает объем V1, имеет давление р1 и находится при температуре T1,. Эта же масса газа в другом произвольном состоянии характеризуется параметрами p2, V2, T2. Переход из состояния 1 в состояние 2 осуществляется последовательно изотермическим (1-1') и изохорным (1'-2) процессами. По законам Бойля-Мариотта и Гей-Люссака.
Исключая
По закону Авогадро, при одинаковых р и Т моли всех газов занимают одинаковый молярный объем Vμ. Уравнение состояниядля моля идеального газа: pVμ = RT, где константа R = 8,31 Дж/(моль·К) — называется |
|
 .
.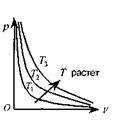 5. Закон Бойля-Мариотта.
5. Закон Бойля-Мариотта.

 — это масса одного моля вещества. Отсюда:
— это масса одного моля вещества. Отсюда: 
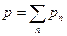

 ,V0 и p0 — объем и давление при t= 0°С;
,V0 и p0 — объем и давление при t= 0°С; . Если начало отсчета сместить в эту точку, то получим
. Если начало отсчета сместить в эту точку, то получим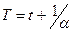 .
. или
или  const при р = const; m = const
const при р = const; m = const или
или  const при V = const; m = const (з-н Шарля),
const при V = const; m = const (з-н Шарля),
 ,
, 
 , получим уравнение состояния идеального газа:
, получим уравнение состояния идеального газа: или
или 