|
|
ЗАНЯТИЕ 8. ДЕЛЕНИЕ МОЛЕКУЛЯРНЫХ СМЕСЕЙМЕТОДАМИ ХРОМАТОГРАФИИ 8.1. Общие замечания.Известно, что основоположник хроматографии М. С. Цвет (1872 – 1919) разделил экстракт пигментов растений (1903) по их сорбции на колонке каолина = белой глины. Т.к. в потоке элюента = жидкости, фильтрующейся через носитель, скорости движения компонентов разделяемых смесей обратны степени их сорбции, Arne Tiselius (1902 – 1971, Швеция) предложил термин «сорбционный анализ» и, стал делить смеси, в зависимостиот времени прохождения элюента через колонку или тонкий слой сорбента с развитой поверхностью. Теоретические основы ионообменной, адсорбционной, распределительной и других видов хроматографии рассмотрены в курсах аналитической и физической химии. Но, т.к. при делении биомолекул, часто одновременно реализуется несколько механизмов, то, не вдаваясь в типы носителей, отметим, что геометрия сорбционного слоя и зависящее от него аппаратное оформление неподвижной фазы, дали ряд вариантов хроматографии (рис 8.1).
Рис. 8.1. Схема методов хроматографии
При плоскостных методах, 1-10 мкл смеси разделяемых веществ наносят на бумагу или тонкий слой сорбента, закрепленный на стекле или фольге. Носитель помещают во влажную, чаще стеклянную камеру с элюентом - смесью двух частично смешивающихся жидкостей. За десятки минут элюент перемещается по сорбенту под действием капиллярных сил и гравитации. При этом одна из жидкостей фиксируется на сорбенте, образуя неподвижную фазу, а другая – подвижная, проходит по нему с большей скоростью. В соответствии со степенью растворимости в той или иной части элюента, компоненты смеси распределяются по хроматограмме. Независимо от принципа деления компонентов, колоночная хроматография возможна вручную, но гораздо удобней специальные приборы – хроматографы. Обычно, при помощи насоса на вход их колонок подают, как разделяемую смесь, так и элюент. А на выходе – размещают детектор, который, независимо от конструкции, в автоматическом режиме непрерывно отражает на диаграмме регистрации = хроматограмме, время выхода и концентрации компонентов в элюате. Варианты колоночной хроматографии (рис. 8.1) отличаются друг от друга не так диаметром, длиной колонки и типом носителя, как очередностью подачи в нее элюента и разделяемой смеси. Преимущество проявительной хроматографии состоит в том, что колонка не требует регенерации, а зоны компонентов анализируемой смеси – разделяются слоями элюата. Из таблицы 8.1 видно, что в соответствии с агрегатным состоянием подвижной фазы, различают газо-жидкостную = ГЖХ и жидкостную хроматографию. Последняя – наиболее разнообразна, т.к. включает в себя фильтрацию в гелях, аффинную и высокоэффективную жидкостную хроматографию = ВЭЖХ, больше известную как HPLC = High pressure liquid chromatography, то есть хроматография под давлением. Т.о., все разнообразие методов хроматографии, как совокупности научных и производственных технологий в разных областях химии, медицины, экологии и т.д., основано на различиях в скоростях движения концентрационных зон компонентов изучаемых смесей, смещающихся относительно сорбента в потоке подвижной фазы. Таблица 8.1 Фазовые отношения в хроматографии
8.2. Дополнительная литература 8.2.1. Справочник по физико-химическим методам исследования объектов окружающей среды. Под ред. Г. И. Арановича и др. – Л.: Судостроение, 1979. – 648 с. 8.2.2. Лабораторное руководство по хроматографическим и смеж-ным методам в 2-х тт. / Под ред. В. Г. Берёзкина. – М.: Мир, 1982. 8.2.3. Остерман Л. А. Хроматография белков и нуклеиновых кислот. – М.: Наука, 1985. – 534 с. 8.2.4. Аффинная хроматография. Методы. – М.: Мир, 1988. – 278 с. 8.2.5. Зеленин К. Н. и др. Нобелевские премии по химии за 100 лет. – СПб.: Гуманистика, 2003. – 218 с. 8.2.6. http://www.krugosvet.ru/articles/114/1011465/print.htm
Экспериментальная часть 8.3.1. Хроматография аминокислот и пептидов на бумаге Принципы метода: 1. Смесь двух частично смешивающихся жидкостей, одна из которых – вода, а другая – водонасыщенный органический растворитель, например фенол или н-бутанол, движутся по капиллярам бумаги с разными скоростями, т.к. полярная вода, связываясь с полярной же целлюлозой носителя, создает неподвижную фазу. Напротив, менее полярный органический растворитель движется по бумаге быстрей и служит подвижной фазой. 2. От обычной фильтровальной, хроматографическую бумагу отличает лишь большая (до 22 %) способность к связыванию воды. 3. В зависимости от направления движения смеси по носителю, различают одномерную радиальную, восходящую, нисходящую и двумерную хроматографию. 4. Соответственно структуре своих радикалов, α-аминокислоты и низкомолекулярные пептидылучше растворяются в той или иной фазе элюента и, как вариант распределительной хроматографии, тоже движутся по носителю с разными скоростями. 5. Экспериментально найдено, что деление аминокислот и пептидов идет эффективней в трехкомпонентных системах растворителей, так как добавки кислот, оснований, спиртов и др., с одной стороны, повышают гидрофильность подвижной фазы, а с другой – изменяют диссоциацию кислых и основных групп компонентов разделяемой смеси. 6. Выявление = индикацию всех компонентов смеси ведут, опрыскав высушенную хроматограмму из пульверизатора, раствором нингидрина, флуорескамина или о-фталевого диальдегида. Два последних индикатора, в присутствии восстановителей образуют с первичными аминами флуоресцирующие продукты, повышая чувствительность метода до 10-9 – 10-11 моля. 7. Выявленные пятна идентифицируютсравнением со «свидетелями» = чистыми образцами изучаемых веществ и, с помощью расчета коэффициентов подвижности: Rf = a/b, где а и b, соответственно, расстояния в миллиметрах, пройденные веществом и фронтом растворителя. Для данной системы растворителей, величина Rf каждого компонента – const. Ход работы: 1. Избегая вероятного проявления отпечатков собственных пальцев, кожа которых секретирует много свободных аминокислот, взять за ребра бумажный диск или квадрат хроматографической бумаги, стороны которого немного больше диаметра чашки Петри и, поместить его на чистый лист своей лабораторной тетради. 2. С помощью линейки и тонко отточенного простого карандаша, без нажима, разделить диск на 4 – 6 примерно равных секторов. 3. Исходя из толщины круглых карандашей – 8 мм, его острием сделать в центре диска отверстие диаметром 6-8 мм. 4. Отступив от края отверстия на 5-10 мм, в каждом секторе поставить заметные точки старта, учитывая, что графит, препятствует растеканию водных растворов! Сбоку обозначить точки цифрами 1, 2, 3 и т.д., а на краю или в углу листа, указать № или инициалы владельца хроматограммы. 5. Положить диск на керамическую поверхность стола и, заполняя соответствующие графы таблицы протокола, нанести капиллярами на точки старта по капле 0,4 % растворов смеси аминокислот и «свидетелей» – аланина, лейцина, лизина, глутаминовой кислоты и дипептида.
6. Пока влажные пятна хроматограммы высыхают на воздухе, свернуть из полоски фильтровальной бумаги шириной 10-15 мм «ножку» или «фитиль» и вставить его в отверстие диска. 7. Открыть чашку Петри с ~10 мл смеси растворителей н-бутанол : уксусная кислота : вода в соотношении 4:1:5 и положить на ее края высушенный диск, проследив, чтоб ножка погрузилась в смесь растворителей. 8. Прикрыть систему крышкой чашки Петри, засечь время начала хроматографии и периодически контролировать движение фронта растворителя по бумаге. 9. Дождавшись подхода растворителя к краям бумаги, снять крышку чашки Петри и, пинцетом уложить на нее влажный диск, отметив в протоколе температуру помещения и время хроматографии. 10. Удалив ножку, высушить хроматограмму в сушильном шкафу при 90-100 С, в течение 10 мин. 11. Опрыскать хроматограмму 0,2 % раствором нингидрина в 96 % этаноле и повторно высушить ее в течение 5 мин. 12. Измерить в мм расстояние, пройденное фронтом растворителя от точки старта и занести его в таблицу протокола занятия. 13. Промаркировав карандашом середину каждого пятна хроматограммы, измерить расстояния их пробега от точек старта, занося результаты в таблицу протокола. 14. Рассчитать для каждого из пятен величину коэффициента распределения = Rf и занести результаты в таблицу протокола занятия. 15. Подтвердить результаты идентификации пятен смеси аминокислот, сравнив их положения со «свидетелями». 16. По мере возможности сделать выводы о влиянии температуры среды на скорость хроматографии и, взаимосвязи структуры аминокислот с их подвижностью в данной системе растворителей.
8.3.2. Гель-хроматография смеси на колонке Сефадекса G – 50 Принцип метода:Разделение смесей этим способом основано с одной стороны, на различиях в размерах их молекул, а с другой - на соизмеримости разделяемых молекул с размерами пор гранул гелей (рис. 8.2). Поэтому крупные макромолекулы в поры геля не проникают и элюируются с колонок первыми. Напротив, чем мельче размеры молекул других компонентов смеси, тем чаще они попадают через поры в гранулы и, задерживаясь в колонке, выходят из нее позже, то есть в больших объемах элюата. Отсюда синонимы метода: гель-фильтрация или метод молекулярных сит.
Рис. 8.2. Схема гель-фильтрации двухкомпонентной смеси (по http://www2.usu.ru/biology/plant_phys/posob_bio_cont.htm)
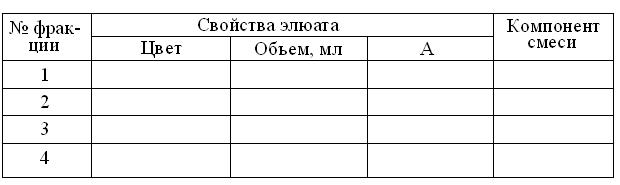
Свойства молекулярных сит имеют многие пористые материалы, начиная с природных или искусственных цеолитов, полиакриламида и пористого стекла, несжимаемых при гидростатическом давлении. Напротив, трехмерные гели агарозы и декстрана (коммерческие названия Сефадекс – Pharmacia, Швеция; Молселект – Reanal, Венгрия), благодаря высокому содержанию гидроксильных групп легко набухают, но и сжимаются при избытке давления или скорости истечения элюата, что нежелательно, во избежание регенерации колонки! Как правило, большие марки препаратов, идущих за их названием, отражают большую степень набухаемости и более крупный размер гранул, при меньшей степени их поперечной сшитости, позволяющих разделять вещества в широком диапазоне молекулярных масс. Ход работы: 1. На входе в колонку 0,9 x 15 см, заполненную гелем Сефадекса G – 50 (Pharmacia, Швеция) удалить пробку и, контролируя положение колонки в штативе с двух взаимно перпендикулярных позиций, довести его зажимами штатива до строго вертикального. 2. Убедившись, что поверхность геля строго горизонтальна и прикрыта фильтром, отрегулировать винтовым зажимом скорость истечения элюата в стакан-приемник до 10 – 15 капель/мин. 3. Дождавшись впитывания элюента на входе в колонку, не допуская подсыхания и взмучивания носителя, пипеткой по каплям, осторожно нанести на гель 0,5 мл смеси (1:1) 0,5 % раствора декстрана голубого (M = 2000 кДа) и насыщенного раствора рибофлавина (M = 376 Да). 4. Параллельно, заменить на выходе из колонки стакан-приемник, штативом с мерной центрифужной пробиркой № 1. 5. Как только делимая смесь впитается в гель, осторожно наслоить на него 5 мл физиологического раствора (0,85 % хлорид натрия) и повторять эту процедуру в течение всего опыта (30 – 40 мл). 6. Ориентируясь на изменения цвета элюата, продвигать под колонкой штатив, собирая тем самым в центрифужные пробирки №№ 1-4, его бесцветную, голубую, бесцветную и жёлтую фракции. 7. В соответствии с Инструкцией по эксплуатации фотоэлектроколориметра модели КФК-2. (п. 4.3.1. данного пособия), включить прогрев ФЭКа. 8. Убедившись, что колонка достигла исходного состояния, снова заменить штатив стаканом-приемником и, дополнительно промыть ее 10-15 мл физраствора. 9. Перекрыть зажимом выход колонки, оставив над поверхностью геля 1,5-2 мл элюента и закрыть вход в нее пробкой. 10. Определить объёмы полученных фракций элюата и занести результаты в таблицу протокола: Результаты гель-фильтрации смеси на колонке 0,9 х 15 см Сефадекса G-50
11. В соответствии с вышеупомянутой (п. 7) инструкцией, измерить против воды абсорбцию полученных фракций элюата при зеленом светофильтре (λ=540 нм) в кювете толщиной 5 мм, занося результаты в таблицу. 12. Построить график элюции с колонки, отложив по оси абсцисс объёмы элюата в мл, а по оси ординат – найденные величины А. 13. На основании данных эксперимента – идентифицировать компоненты исходной смеси.
Вопросы для самоконтроля 8.4.1. Что такое хроматография, где и зачем ее применяют? 8.4.2. Объясните термины: сорбция, носитель, подвижная и неподвижная фазы, элюент, элюат. 8.4.3. Укажите сходство и основные различия между хроматографией в тонких слоях и колонках. 8.4.4. Объясните термины хроматограмма, детектор, коллектор фракций. 8.4.5. Объясните, чем различаются газо-жидкостная и жидкостная хроматография? 8.4.6. Какие варианты жидкостной хроматографии вам известны? 8.4.7. Какие принципы лежат в основе бумажной хроматографии и, чем хроматографическая бумага отличается от обычной фильтровальной? 8.4.8. Объясните преимущества и недостатки бумажной хроматографии по сравнению с другими видами ТСХ? 8.4.9. Объясните, на каких принципах основано разделение аминокислот и пептидов в трехкомпонентных системах растворителей? 8.4.10. Объясните понятия «индикация», «идентификация», «свидетели», Rf , «коэффициент подвижности»? 8.4.11. Объясните принципы гель-хроматографии и укажите ее синонимы. 8.4.12. Какие материалы имеют свойства молекулярных сит? 8.4.13. По каким признакам можно идентифицировать компоненты фракций, элюируемых с колонки? 8.4.14. Молекулярная масса бычьего сывороточного альбумина = БСА, по данным гель-хроматографии составляет 70 кД. Рассчитайте, сколько остатков триптофана содержит молекула БСА, если молекулярная масса триптофана - 204 Да, а его содержание в этом белке составляет 0,68 %.
Задание на дом 8.5.1. При подготовке к занятию 9 объясните роль ДНК-реплика-тивного комплекса в жизненном цикле клеток. Укажите стехиометрию реакций биосинтеза ДНК. 8.5.2. Что вы знаете об идентичности ДНК и роли теломераз в контроле клеточного цикла многоклеточных организмов? 8.5.3. Почему и какие повреждения ДНК возможны в клетках? Что вы знаете о механизмах молекулярных мутаций и механизмах их репарации? 8.5.4. Мобильные генетические элементы и типы рекомбинаций, как основа инфекций, наследственной изменчивости и эволюции. 8.5.5. Современные представления о механизмах канцерогенеза. 8.5.6. Стехиометрия реакций и роль РНК-полимеразного комплекса в процессе транскрипции. Сигналы инициации и терминации в ДНК-матрице. 8.5.7. Понятие о первичных транскриптах и роли микро-РНК в посттранскрипционном процессинге транспортных, рибосомных и матричных РНК. 8.5.8. Биологический код и его свойства. Представления об «идеальном» генетическом коде митохондрий. 8.5.9. Эволюция рибосом и инициации трансляции. 8.5.10. Структура и последовательность реакций аминоацил-тРНК-синтетаз = АРСаз, обеспечивающих надежность узнавания. Представления об изоакцепторных т-РНК. 8.5.11. Последовательность событий инициации, элонгации и терминации трансляции. Принцип контроля времени распада матричных РНК. 8.5.12. Бесклеточные белоксинтезирующие системы. Представления о маркерах стадий онтогенеза и процессов адаптации. 8.5.13. Локализация и основные этапы фолдинга полипептидов. 8.5.14. Теория оперонов в экспрессии генов прокариот. Адаптационные механизмы индукции и репрессии. Энхансеры = усилители и силенсеры = гасители операторных участков гена. 8.5.15. Механизмы управления трансляцией в клетках эукариот: альтернативный процессинг мРНК, ее транспорт в цитозоль и контроль стабильности молекул. 8.5.16. Если волос человека растет на 15-20 см/год, рассчитайте, сколько пептидных связей должно образоваться в α-кератине для удлинения волоса на 1 см, если известно, что α-кератин эпителиоцитов позвоночных целиком состоит из α-спирали, шаг которой 0,54 нм, а длина - 3,6 аминокислотного остатка. Какова при этом скорость образования пептидных связей? |
|