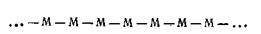|
|
Общая характеристика растворов высокомолекулярных соединений.К высокомолекулярным соединениям относится обширный класс веществ, основным признаком которых является высокая молекулярная масса (от 10 000 до нескольких миллионов) и, следовательно, большой размер молекул. Как показывает опыт, свойства высокомолекулярных соединений, а также их растворов определяются не только химическим составом, но и размерами и формой макромолекулы. От величины и формы молекул соединений зависят прочность, гибкость, эластичность, устойчивость к многократным деформациям и ряд других важнейших технических свойств изделий, получаемых из них, при сравнительно невысокой плотности. Все высокомолекулярные соединения делятся на две группы: природные (натуральный каучук, естественные смолы, целлюлоза, белки, крахмал, камеди) и искусственные (искусственные смолы, различные пластические массы, производные целлюлозы, синтетические каучуки). Иногда высокомолекулярные вещества подразделяются не на две, а на три группы: природные, искусственные и синтетические. В группу синтетических соединений входят все полимеры, полученные путем синтеза низкомолекулярных веществ (капрон, найлон, полиэтилен). К числу искусственных высокомолекулярных веществ относятся соединения, получаемые в результате химической обработки природных высокополимерных соединений (в большинстве случаев это производные целлюлозы). С геометрической точки зрения все разнообразие форм макромолекул высокомолекулярных соединений может быть сведено в основном к трем типам: линейной, двухмерной (или плоскостной) и пространственной, т. е. трехмерной. Линейными называются такие полимеры, макромолекулы которых существуют в виде длинных неразветвленных цепей. Строение линейной макромолекулы можно схематически представить так:
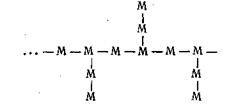
где М — мономерная единица. Такой тип строения макромолекул имеют многие высокомолекулярные органические соединения, в которых основной связующей единицей является четырехвалентный атом углерода. Очень часто линейные цепи дают боковые ответвления, и тогда они называются разветвленными. В этом случае макромолекулу можно отнести к типу двухмерных полимеров. Схематически разветвленную цепь макромолекул можно представить так:
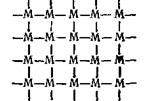
В более редких случаях однородные линейные макромолекулы под влиянием особых факторов (температуры, различных добавок) могут вступать друг с другом в тесную химическую связь, устанавливающуюся в отдельных участках цепи по ее длине в виде своеобразных «мостиков» и «перемычек»:
Такие макромолекулы получили в литературе название «сшитых» макроструктур. Поскольку «сшивание» идет в пространстве, образующиеся макромолекулы носят трехмерный характер. Растворы высокомолекулярных соединений, несмотря на общность некоторых свойств с истинно коллоидными лиофобными растворами, имеют свои специфические особенности. Эти отличия связаны тремя общими термодинамическими признаками, характеризующими любой истинный раствор: 1) самопроизвольностью образования растворов ВМС; 2) высокой степенью их устойчивости; 3) обратимостью происходящих в них процессов. Всякий лиофобный (гидрофобный) золь получается только искусственным путем за счет приложенной извне работы (химической или механической). Именно за счет этой работы золь и обладает большим избытком свободной поверхностной энергии, которая стремится к уменьшению, чем и обусловлена его агрегативная неустойчивость. Растворы высокомолекулярных соединений могут образоваться самопроизвольно в результате неограниченного набухания, переходящего далее в обычное растворение, в результате чего происходит не увеличение, а убыль свободной энергии. Эта важная особенность высокомолекулярных соединений объясняется весьма большой способностью молекул взаимодействовать с дисперсионной средой, что, собственно, и явилось причиной для употребления термина лиофильность. Именно с лиофильностью связаны и свойства большой сольватируемости и растворимости высокомолекулярных соединений по сравнению, например, с рассмотренными ранее гидрофобными коллоидами. Эта особенность и обусловливает довольно редкие различия между лиофобными золями и растворами ВМС. Если лиофобные золи могут существовать без видимых изменений только в очень незначительных концентрациях и поэтому обладают вязкостью, мало отличной от вязкости чистой дисперсионной среды, и проявляют свои диффузионные и осмотические свойства в ничтожной степени, то растворы высокомолекулярных соединений могут длительно существовать в достаточно ощутимых молярных концентрациях, следовательно, обладают заметным осмотическим давлением и повышенной вязкостью. Лиофобные золи являются системами агрегативно неустойчивыми, растворы же высокомолекулярных соединений способны сохранять свою молярную концентрацию очень долгое время, т. е. являются системами термодинамически устойчивыми. Это экспериментально подтвердил В. А. Каргин, который показал, что растворы ВМС подчиняются, как и истинные растворы, правилу фаз. И, наконец, в тесной и неразрывной связи со всем вышеизложенным находится и третий признак растворов ВМС —это обратимость всех совершающихся в них процессов с изменением температуры, давления и концентрации. Напомним, что все эти процессы являются необратимыми для лиофобных (гидрофобных) коллоидов. Высокомолекулярные соединения способны образовывать не только истинные растворы, но и типичные лиофобные золи, если в качестве дисперсионной среды взята жидкость, по отношению к которой высокомолекулярное вещество является лиофобным. Такие коллоидные растворы отличаются ясно выраженной лиофобностью, что выражается в слабом взаимодействии вещества дисперсной фазы с дисперсной средой, требуют обязательного наличия стабилизатора для создания агрегативной устойчивости, обладают слабой диффузией и очень малым осмотическим давлением. Так же как и лиофобные золи, коллоидные растворы ВМС обладают термодинамической неустойчивостью, вызванной значительным избытком поверхностной свободной энергии. Таким путем можно получить типичные лиофобные золи из желатина и спирта, из нитроцеллюлозы и воды.
|
|