|
|
Теоретическая часть. Растворы: типы и области применения.Лабораторное занятие №2. Строение и функции биополимеров. Физико-химические свойства. Качественный анализ.
Теоретическая часть. Растворы: типы и области применения.
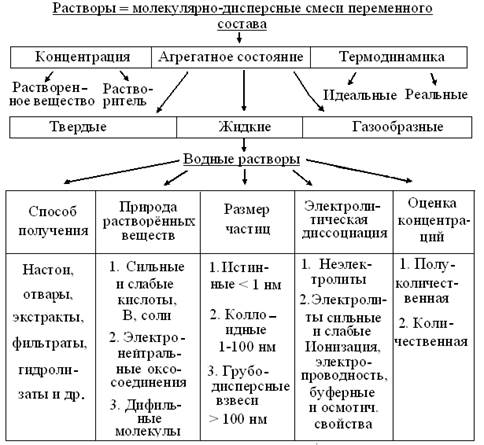
Известно, что системы с концентрационным преобладанием одного из компонентов называют растворами. Исходя из конкретных свойств, важных в данное время, их рассматривают с разных позиций (рис. 1). Если термин употребляют без уточнений, обычно имеют в виду жидкие растворы. Но, т.к. из всех жидкостей, на Земле и в биосфере преобладает вода, то чаще всего в быту, технике и биологии встречаются водные растворы веществ.
Рис. 1. Схема подходов к растворам
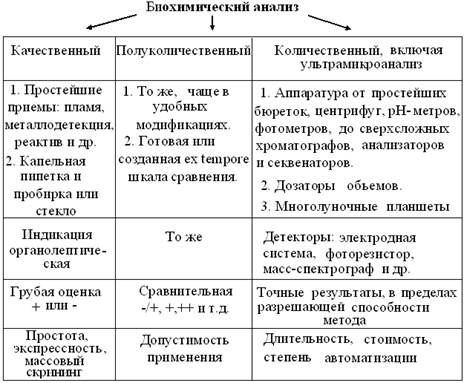
Очевидно, что в зависимости от конкретных задач, есть 2 принципиально разных способа получения растворов: из природного, чаще растительного сырья и, навесок чистых препаратов. Как известно, большинство водных растворов готовят с помощью обычной мерной посуды, ускоряя при необходимости их растворение нагревом систем в конических колбах. Но, при растворении биополимеров нужно учитывать возможность их частичной или полной денатурации, в том числе, и от контакта полимера со стеклом или интенсивного перемешивания. Кроме того, лиофилизированные препараты биополимеров очень летучи, создавая неудобства при взвешивании и редко растворяются в дистилляте. Наконец, как известно, растворению полимеров всегда предшествует стадия набухания их молекул. Поэтому их растворы готовят накануне применения, с помощью рекомендованных и охлажденных буферных смесей и пластиковой посуды, избегая интенсивного перемешивания и образования пены, после чего - хранят в холодильнике. Из схемы 1 также видно, что независимо от способа получения, природа растворенных веществ прямо определяет размер частиц и степень гомогенности раствора, его оптические и кинетические свойства. При этом, степень склонности веществ к электролитической диссоциации, соответственно сохраняет или повышает количество частиц в растворе. В последнем случае, ионы разных знаков обеспечивают раствору новое свойство электропроводности. Наконец, часть, не менее чем трехкомпонентных систем электролитов, способных поддерживать постоянство рН при добавлении сильных кислот или оснований, называют буферными растворами. При полуколичественных оценках концентрации пользуются терминами: разбавленный, насыщенный – это рассол или пересыщенный растворы. К большинству водных растворов применимы правила: 1. В 1 мл – 20 капель, то есть объем капли ~50 мкл. 2. Объем чайной ложки – 5 мл, десертной – 10 мл, столовой – 15 мл. При количественном подходе, обычно используют массовые, молярные или объемные доли вещества, относительно общего количества системы. Согласно Международной системе единиц (СИ), допустимы лишь массовые (г/м3) и молярные (моль/м3) концентрации и их производные. Но, в обиходе, они слишком велики, трудоемки и неудобны, так как требуют пересчетов, специального оборудования и навыков работы. Поэтому, во всех допустимых случаях лабораторной и фармацевтической практики, применяют технически более простые и удобные объемные доли: г/л, ммоль/л, г/дл, мг/мл и т.п. При титриметрии пользуются более редкими величинами выражения концентраций: «титр» и «нормальность» (н.), отражающими, соответственно, количество граммов растворенного вещества в 1 мл или число химических эквивалентов растворенного электролита в 1 л. раствора. В быту и технике часто приемлемы более грубые, но технически простые и быстрые приемы выражения концентраций в процентах (%) или промилле (‰), соответственно массовой или объемной доле на 100 или 1000 мл раствора. Наконец в гомеопатии, концентрации растворов часто выражают долями на млн-1, трлн-1 и т.д., вплоть до числа Авогадро. Из схемы (рис. 2) следует, что кроме общеизвестных методов качественного и количественного анализа, современная биохимия и молекулярная биология применяет и другие подходы. Известно, что качественный анализ основан на органолептических свойствах выявляемых компонентов, исходя из которых различают: внешний вид и запах вещества, выделение пузырьков газа, изменения цвета = цветные реакции, появление осадков в растворе = осадочные реакции, звуковой сигнал металлодетектора, изменения цвета пламени и т.п. Его классический пример – закрепившийся в органической химии способ описания веществ, начиная с их внешнего вида и физических свойств. Техническая простота и Экспрессность качественного анализа, часто допускают его применение как в лабораториях, так и на месте (on site), то есть в быту и полевых условиях. Примером этого, может быть оценка качества шерсти по запаху серы подожженной нити. Простые и дешевые приемы качественного анализа образцов в сжатые сроки, без предварительной подготовки проб, легли в основу методологии массового скрининга – просеивания (screen, англ. – сито). Такая экспресс-оценка полезна не только при металлодетекции, но и для выявления наследственных болезней у новорожденных, изучения токсичности и экологической безопасности образцов атмосферы, почв, воды, пищевых продуктов, косметики, бытовых изделий и т.д. Методы скрининга должны полностью исключать отрицательные результаты химико-биологических тестов, которые считают окончательными без дополнительной проверки. Напротив, все пробы с положительной реакцией, в т.ч. и ложноположительной, изучают далее, с помощью более информативных методов количественного анализа.
Рис. 2. Характеристика типов анализа в биологии и медицине
Количественный анализ гораздо более трудоемок, так как связан с правильным выполнением технически громоздких операций подготовки образцов, применением мерной посуды, аналитических весов, рН-метров, фотометров и других сложных и сравнительно дорогих приборов. Понятно, что все эти требования выполнимы, лишь при наличии квалифицированного персонала и условий стационарной лаборатории. Тем не менее, в настоящее время, до 90 % полезной информации в экологической, медико-санитарной, сельскохозяйственной и судебной диагностике, получают с помощью аппаратурных методов количественного анализа. Часть этих методик осваивается при дальнейшем прохождении курса. Меньше известен, издавна популярный в медико-биологических науках, полуколичественный анализ. Как и количественный, он основан на какой-либо качественной реакции, интенсивность которой пропорциональна содержанию искомого вещества. Как правило, он не позволяет оценить его абсолютное содержание, но, наличие или возможность самостоятельного построения шкалы сравнений, делают этот способ технически приемлемым, относительно экспрессным и довольно экономичным, позволяя быстро оценивать серии образцов по принципу больше/меньше. Простейший пример полуколичественного анализа – универсальная индикаторная бумага, позволяющая быстро и просто получить примерный ответ о величине рН исследуемого раствора. 2. Дополнительная литература 1. Золотов Ю. А. Тест-методы // Ж. аналит. Химии, 1994. – Т. 49, № 2. – С. 149 - 157. 2. Евгеньев М. И. Тест-методы и экология // Соросовский образовательный журнал, 1999. – №11. – С. 29-34. 3. Максимовский Л. Ф., Микичур Н. И. Методы микроманипуляций и ультрамикроанализа в биологии и медицине. – Новосибирск.: Наука, 1989. – 236 с. 4. Хиллман Г. Определенность и неопределенность в биохимических методах. – М.: Мир, 1975. – 160 с. 5. Геккелер К., Х. Экштайн Аналитические и препаративные лабораторные методы. – М.: Химия, 1994. – 416 с. 6. Манниатис Т. и др. Молекулярное клонирование. – М.: Мир, 1984. – 480 с.
Экспериментальная часть. |
|