|
|
Определение изоэлектрической точки белкаВ изоэлектрической точке растворы белков неустойчивы. Молекулы белка с одинаковым количеством положительных и отрицательных зарядов легко выпадают в осадок. Значение рН, соответствующее изоэлсктрической точке, является характерным для каждого белка. Например, для казеина рН равно 4,7, для яичного альбумина - 4,8, желатина - 4,9, зеина (кукурузного белка) - 6,2; у протаминов и гистонов изоэлектрическая точка лежит в слабощелочной среде. Выпадение белка в осадок в изоэлектрической точке можно ускорить добавлением водоотнимающих веществ (спирта, ацетона, эфира) или танина. Одни из них (органические растворители) уменьшают степень гидратации белковых макромолекул, разрушают их водные оболочки, другие, как, например, танин, образуют нерастворимые в воде соединения с азотистыми гетероциклическими группировками. Реактивы: а) желатин, 0,5 % раствор; б) уксусная кислота, 0,1 н раствор; в) уксуснокислый натрий, 0,1 н раствор; г) этиловый спирт, 96%-ный; д) танин, 0,1%-ный раствор. В пять пробирок наливают растворы уксусной кислоты и уксуснокислого натрия в количествах, указанных в табл. 4, после чего в каждую пробирку добавляют по 1 мл раствора желатина и хорошо перемешивают, затем прибавляют по 4 мл этилового спирта (или по 1 мл раствора танина) и снова перемешивают. Через 5-10 мин. просматривают все пробирки и оценивают степень мутности смеси в каждой из них. рН наиболее мутной смеси соответствует изоэлсктрической точке желатина. Результаты опыта записывают в таблицу, которую составляют по образцу табл. 4. Таблица 4. Определение изоэлсктрической точки белка
Контрольные вопросы 1. Что такое «растворы» и как их можно классифицировать? 2. От чего зависят свойства водных растворов? 3. Какие вещества растворяются в воде? 4. Чем различаются растворение низкомолекулярных веществ и биополимеров? 5. Как влияют размеры растворенных частиц на свойства растворов? 6. В чем смысл деления растворов на электролиты и неэлектролиты? 7. Какие способы оценки концентрации растворов вы знаете? 8. В соответствии с предложенным шаблоном, опишите свойства растворов, как дисперсных систем
9. Чем объяснить высокую способность воды к растворению веществ? 10. Чем различаются понятия «гидратация», «набухание» и «растворение» веществ в воде? 11. Сгруппируйте типы веществ, способных растворяться в воде. В чем заключаются различия в их растворении? 12. Оцените средние размеры малых и полимерных биомолекул. 13. Чего больше в организме, внеклеточной или внутриклеточной воды? 14. От чего зависит содержание внеклеточной воды в организме? 15. Наибольшее количество воды содержит: а) цитозоль, б) эндоплазматическая сеть, в) рибосомы, г) митохондрии, д) ядро. 16. Известно, что спринтеры перед стартом интенсивно и глубоко дышат ~30 секунд, добиваясь гипервентиляции легких и удаления из них СО2. Почему при этом, рН крови может достигать 7,6? 17. В соответствии с предложенным шаблоном, заполните таблицу характеристики 4-х основных классов малых биогенных молекул = биомономеров. По какому принципу шла их селекция?
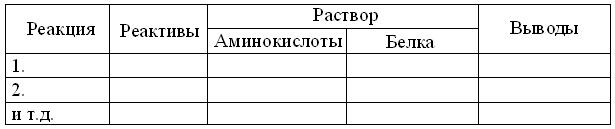
18. Оформляя протокол к лабораторному занятию, соответственно шаблону, на развороте лабораторной тетради вычертить таблицу, для суммирования результатов качественных реакций:
19. Какие типы биохимического анализа вам известны и чем они различаются? 20. Что такое скрининг, на чем он основан и для чего применяется? 21. Чем различаются полуколичественный и количественный анализ? 22. Расскажите о специфических качественных реакциях на аминокислоты и белки. 23. Укажите известные вам цветные и осадочные реакции на аминокислоты и белки. 24. Как обнаружить аминокислоты и белки в образцах? 25. Можно ли предположить, по аналогии, с аминокислотами и белками, существование качественных реакций для мономеров и полимеров других классов биомолекул? 26. Назовите основные факторы, обуславливающие стабильность молекул белка в растворе. 27. Причины осаждения белков нагреванием при рН около 7,0? 28. Характеристика обратимых и необратимых реакций осаждения белков. 29. Почему в растворе при рН<7,0 белки при нагревании не выпадают в осадок? 30. Почему в растворе при рН>7,0 белки при нагревании не выпадают в осадок? 31. Почему в растворе при рН<7,0 с добавлением хлорида натрия белки при нагревании выпадают в осадок? 32. Механизм действия минеральных кислот на молекулы белков в растворе. 33. Механизм осаждения белков органическими кислотами. 34. Механизм осаждения белков солями тяжелых металлов. 35. Механизм осаждения белков органическими растворителями. 36. Изоэлектрическая точка аминокислот, пептидов и белков. Методы определения. 37. Методы выделения очистки белков. 38. Объясните, чем различаются понятия «аминокислоты», α-аминокислоты и «протеиногенные» аминокислоты? 39. По каким признакам стоит классифицировать α-аминокислоты? 40. Как соединяются α-аминокислоты в пептидах и белках? 41. Что вы знаете о номенклатуре пептидов? 42. Объясните термин «код» и подумайте, какие коды в биохимии вам известны? 43. Откуда возникла потребность в кодах аминокислот? 44. Запишите брутто-формулы и оцените растворимость каждой, из нижеследующих пар пептидов: 45. (Гли)20 и (Глу)20 при рН 7,0; 46. (Лиз-Ала)3 и (Фен-Мет)3 при рН 7,5; 47. (Ала-Сер-Гли)5 и (Ала-Сер-Гис)5 при рН 9,0; 48. (Ала-Асп-Гли)5 и (Асн-Сер-Гис)5 при рН 3.0. 49. Попытайтесь составить функциональную классификацию внутри- и внеклеточных пептидов. 50. Чем различаются структура, свойства и биологическая роль пептидов и белков? Почему разнообразие белков гораздо больше, чем у пептидов? 51. Какие виды гидролиза белков Вам известны? 52. Определите понятия денатурация и ренатурация = ренативация белков. Чем они отличаются от гидролиза? Расскажите об известных вам признаках и условиях осаждения белков из растворов. 53. Если изоэлектрическая точка = ИЭТ пепсина лежит при рН 1, то какие функциональные группы R и, каких именно аминокислот, могут обеспечить это свойство? 54. Какие функциональные группы и, каких именно аминокислот, нужны протаминам и гистонам, чтоб обеспечить ИЭТ > 10? 55. Общая характеристика пептидов, полипептидов, белков и их строения. 56. Как соединяются аминокислоты в молекуле белка и за счет каких групп? Соедините Ала, Цис, Сер. 57. Перечислите цветные реакции на белки и аминокислоты. 58. Какая реакция открывает пептидные связи? Её химизм. 59. Что характеризуют цвет и интенсивность окраски при положительной биуретовой реакции? 60. Что открывает нингидриновая реакция? Её химизм. 61. Назовите аминокислоты имеющие в радикале бензольное кольцо. Какой реакцией можно обнаружить ароматические аминокислоты? Её химизм. 62. Назовите аминокислоты содержащие серу. Какую из них обнаруживает реакция Фоля? Химизм реакции. 63. Исходя из структуры белков объясните, почему при «горячей» стирке и сушке, изделия из шерсти «садятся», а из шелка – нет? 64. Можно ли считать основой биоразнообразия, видоспецифичность множества гомологичных белков? 65. Какую цветную реакцию используют для количественного определения белков в растворе и почему? 66. Какую цветную реакцию используют для количественного определения α-аминокислот и почему? Какие вещества называются белками? 67. Чем обусловлены цветные реакции на белки? 68. Что вы можете сказать об аминокислотном составе белков, если с раствором одного из них реакции Миллона и ксантопротеиновая положительны, а с раствором другого отрицательны? 69. Как с помощью цветных реакций обнаружить в белке аргинин? Как обнаружить в белке цистеин? Как обнаружить в белке тирозин? 70. В соответствии с предложенным шаблоном, заполните таблицу факторов и механизмов денатурации:
Тестовые задания: 1) Какие из предложенных соединений образуют в щелочном растворе биуретовый комплекс меди? а) Asp; Ser; Cys; Met; Met-Thr-Phe б) Ser-Cys-Ala; Gly; Val; Leu; Trp-Tyr в) Ser; He; Glu-Met; Leu-Ala; Gly-Leu- Ala г) Trp-Trp-Tyr; His; Lys; Pro-Pro; Pro д) Phe-Tyr-Ala; Arg; Asn; Gln-Arg; Lys е) Asp-Asn-Ala; Phe; Trp; Pro-Val; Leu ж) Ser-Ile; Gly-Arg-Gly; Pro; Phe; Met з) Asp-Ile-Leu; Asp; Ala-Thr; Gly, Pro и) Cys; Met; Val; Trp-Ala-Thr; Gly-Met-Cys к) Ser; Met-Gly-Arg; Тrp; Pro; Asp 2) Какие из предложенных аминокислот вступают в ксантопротеиновую реакцию? а) Не; Val; Met; Phe; Trp б) Lys; Pro; Phe; Gin; Tyr в) Tyr; Phe; Pro; His; Arg r) Thr; Ser; His; Phe; Trp д) Trp; Pro; Ala; Val; Phe 3) Какие аминокислоты вступают в реакцию с реактивом Фоля? а) Cys; б)Thr; в) Met; г)Val; д) Arg 4) Какие из предложенных аминокислот вступают в реакцию с реактивом Милона: Gly; Val; Не; Туг; Pro ? 5) Для распознавания какой аминокислоты используют в качестве реагента α-нафтол: Glu; Asp; Ala; Met; Arg? 6) Для распознавания какой аминокислоты используют в качестве реагента w-диазобензолсульфокислоту: Thr; Met; Ala; Trp; His? 7) Для распознавания какой аминокислоты используют в качестве реагента глиоксиловую кислоту: Trp; Туг; Gin; Gly; Ala? 8) Для распознавания какой аминокислоты используют в качестве реагента офталевый диальдегид: Leu; Gly; Cys; Met; Asn?
|
|