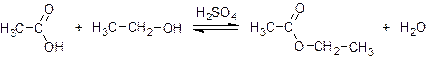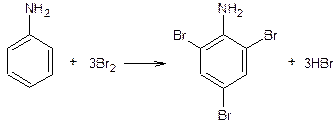|
|
Дробная (фракционная) перегонкаДанный вид перегонки служит для выделения в чистом виде компонентов однородной смеси, обладающих различными температурами кипения. Смесь тем труднее разделяется перегонкой, чем ближе температура кипения отдельных ее компонентов. Для увеличения эффективности разделения смеси, и уменьшения числа перегонок пользуются дефлегматорами. Сущность их действия состоит в том, что вследствие охлаждения наружным воздухом часть паров перегоняемой смеси конденсируется. Сконденсировавшиеся пары, называемые флегмой, стекают обратно в колбу, обогащаясь высококипящим компонентом, а пары, которые летят дальше, обогащены низкокипящим компонентом. Устройство дефлегматоров обеспечивает хороший контакт между стекающей вниз жидкостью (флегмой) и поднимающимся вверх паром. Размеры дефлегматоров выбирают с учетом свойств жидкостей, образующих смесь. Например, для веществ, кипящих ниже 1500С, берут более длинный дефлегматор; для веществ, кипящих выше этой температуры, - более короткой.
Определение показателя преломления Показатель преломления широко используется для идентификациижидких веществ и проверки их чистоты. Показатель преломления n – величина постоянная для данного вещества, равна отношению синусов угла падения света на поверхность раздела двух сред и угла преломления света: n = sin ά / sin β; Показатель преломления зависит от температуры и резко меняется с изменением длины волны света, поэтому измерения проводят при постоянной температуре и монохроматическом свете. Как правило, измерения проводят при 200С и при длине волны, соответствующей длине волны желтой линии натрия Д (λ = 589,3 нм). Символ «nд20» означает, что показатель преломления был определен для линии Д при 200С. Для большинства жидких органических веществ показатель преломления находится в пределах от 1,3 до 1,8. Для определения показателя преломления используют рефрактометр типа ИРФ – 22. Работу проводят следующим образом: открывают верхнее полушарие измерительной головки. Протирают смоченной диэтиловым эфиром (спиртом) ваткой гипотенузные грани осветительной и измерительной призм. Дают эфиру испариться. На плоскость измерительной призмы наносят каплю исследуемого вещества не касаясь призмы пипеткой. Осторожно закрывают верхнее полушарие. Осветительное зеркало устанавливают так, чтобы свет от источника поступал к осветительной призме и равномерно освещал поле зрения. Зеркало ставят так, чтобы свет поступал в окошко, освещающее шкалу прибора. Вращая маховичок и наблюдая в окуляр зрительной трубы, находят границу и тени с перекрестием сетки и снимают отсчет по шкале показателя преломления. Показатель преломления измеряется с точностью до 4 – го знака после запятой. Перед определением показателя преломления исследуемого вещества, прибор проверяют на точность по воде, имеющей nD20 = 1,3333.
Контрольные вопросы по теме «Методы очистки органических соединений» l Назовите методы очистки твердых органических веществ. l Назовите методы очистки жидких органических веществ. l Метод перекристаллизации. Выбор растворителя. Методика проведения перекристаллизации. l Метод возгонки (сублимации). В каких случаях данный метод очистки применим? От чего зависит скорость возгонки? Методика проведения возгонки. l Как оценить степень чистоты кристаллического вещества? Методика определения температуры плавления кристаллического вещества. l Простая перегонка. Для очистки каких органических жидкостей используется данный метод? Из чего состоит прибор для перегонки? Методика проведения простой перегонки. l Для каких целей используют дробную (фракционную) перегонку? Из чего состоит прибор для дробной перегонки? Сущность действия дефлегматора. l Как оценить степень чистоты жидкого органического вещества? Методика определения показателя преломления.
Синтез органических соединений Иодоформ
Реактивы: ацетон – 4 г(5 мл); иод -2 г; иодид калия – 4 г; гидроксид натрия – 10% -ный раствор.
В стакане емкостью 150 мл помещают 4 г иодида калия, приливают 7,5 мл дистиллированной воды и после растворения соли добавляют 2 г иода. К полученному раствору приливают 17, 5 мл воды. Затем в реакционную массу вводят 5мл ацетона и при перемешивании по каплям добавляют из капельной воронки 10%-ный раствор гидроксида натрия до исчезновения красноватой окраски раствора (приблизительно 5-6 мл). Иодоформ, который при этом выпадает в виде желтого кристаллического осадка, через 30 минут отфильтровывают на воронке Бюхнера, промывают небольшим количеством воды и высушивают на воздухе. Выход 0,93 г (90% от теоретического). Иодоформ (трииодметан) – твердое кристаллическое вещество желтого цвета со специфическим запахом и Tплав.190 0C. Растворяется в этиловом спирте, эфире, хлороформе. В воде практически нерастворим, не перегоняется с водяным паром. Быстро гидролизуется раствором щелочи, поэтому следует избегать сильнощелочной среды в процессе синтеза.
Бромэтан
C2H5OH + H2SO4 ↔ C2H5–O–SO3H + H2O
C2H5–O–SO3H + HBr ↔ C2H5Br + H2SO4
Реактивы: этанол (95%) -16 мл; бромид калия -15 г; серная кислота – (ρ =1,84 г/см3)
К 16 мл концентрированной серной кислоты, помещенной в круглодонную колбу емкостью 200 мл, быстро и при постоянном перемешивании приливают 16 мл этанола. После охлаждения до комнатной температуры к реакционной смеси осторожно при перемешивании и внешнем охлаждении приливают 10 мл воды. Затем прибавляют 15 г тонко растертого бромида калия. Воду добавляют с целью подавления побочной реакции – образования эфира - и устранения потери бромоводородной кислоты за счет улетучивания. Для более полного использования бромоводорода этанол берут в некотором избытке. Колбу соединяют с прямым холодильником (установка для простой перегонки), через рубашку которого пропускают сильную струю воды. Бром этан летуч, поэтому его собирают под воду. Конец аллонжа опускают примерно на 1 см в воду с кусочками льда, налитую в приемник. Много воды наливать в приемник не следует, так как бромэтан несколько растворим в ней: при 20 0C в 100 г воды растворяется 0,914 г бромэтана. Снаружи колбу – приемник охлаждают в бане со льдом. Реакционную колбу нагревают, следя за тем, чтобы вспенивающуюся реакционную смесь не перебросило в приемник. Бромэтан отгоняется в виде тяжелых маслянистых капель. Если во время перегонки вода из приемника поднимается в аллонж, приемник опускают настолько, чтобы конец аллонжа лишь немного был погружен в нее. Когда перегонка бромэтана закончится, содержимое приемника переливают в делительную воронку и сливают бромэтан (нижний слой) в сухую колбу. Колбу с бромэтаном охлаждают смесью льда и соли. Осторожно по каплям и при встряхивании добавляют из капельной воронки концентрированную серную кислоту до тех пор, пока она не соберется в виде отдельного слоя под бромэтаном. При обработке серной кислотой из бромэтана извлекаются этанол, диэтиловый эфир (побочный продукт) и вода (происходит высушивание). Бромэтан переносят в сухую делительную воронку, отделяют верхний слой и переносят в колбу для перегонки. Перегонку сухого бромэтана ведут на водяной бане; приемник охлаждают снаружи ледяной водой. Собирают фракцию, отгоняющуюся в интервале 35-40 0C. Выход бромэтана – 12 г. Бромэтан (бромистый этил, этилбромид) – бесцветная жидкость; смешивается со спиртом, диэтиловым эфиром, хлороформом. Tкип. = 38,4 0C; ρ = 1,4555 г/см3;
Уксусноэтиловый эфир
Реактивы: уксусная кислота (ледяная) – 20 мл; этанол -23 мл; конц. серная кислота (ρ = 1,84 г/см3) - 4,6 г; карбонат натрия; хлорид кальция, насыщенный раствор; хлорид кальция безводный.
В колбу Вюрца, снабженную капельной воронкой и соединенную с нисходящим водяным холодильником, помещают 3 мл этилового спирта и 2,5 мл концентрированной серной кислоты. Содержимое нагревают до 140 0C и после достижения этой температуры из капельной воронки начинают медленно приливать смесь 20 мл ледяной уксусной кислоты и 20 мл этилового спирта с такой скоростью, с какой отгоняется образующийся уксусноэтиловый эфир. После окончания отгонки этилацетата его переносят в делительную воронку и промывают насыщенным раствором карбоната натрия для удаления непрореагировавшей уксусной кислоты, контролируя индикаторной бумагой. Эфирный слой отделяют и встряхивают его с насыщенным раствором хлорида кальция для удаления непрореагировавшего спирта (с первичными спиртами хлорид кальция образует кристаллическое молекулярное соединение СаСI2 · 2С2Н5ОН, не растворимое в этилацетате, но растворимое в воде). После разделения слоев в делительной воронке эфирный слой отделяют, сушат безводным хлоридом кальция и перегоняют, собирая фракцию с Ткип 75-79 0C . Выход 20 г. Уксусноэтиловый эфир (этиловый эфир уксусной кислоты, этилацетат) – бесцветная жидкость с приятным запахом. Смешивается со многими органическими растворителями: этанолом, диэтиловым эфиром, бензолом, хлороформом, ограниченно растворяется в воде. Tкип. = 77,15 0C; ρ = 0,9010 г/см3;
Триброманилин
Реактивы: анилин (свержеперегнанный) – 2,5 мл; бром – 4,8 мл; бромид калия – 9 г; соляная кислота (конц.); гидроксид натрия (10%); этанол.
В широкогорлой плоскодонной колбе растворяют 2,5 мл анилина в 75 мл воды с 2,5 мл соляной кислоты. Отдельно в стакане растворяют в 50 мл воды 9 г бромида калия и 4,8 мл брома при перемешивании. Полученный прозрачный раствор выливают в капельную воронку, помещенную над реакционной колбой. Постепенно, по каплям приливают его в течение 30 мин в реакционную смесь при энергичном перемешивании. Реакция галогенирования должна проходить при комнатной температуре. По окончании реакции окраска брома исчезает и выпадает осадок триброманилина. Его отсасывают на воронке Бюхнера, промывают 10%-ным раствором гидроксида натрия, затем большим количеством воды. Влажный триброманилин очищают от примесей кристаллизацией из горячего спирита (около 150 мл). Спиртовой раствор помещают в ледяную баню на 1 час для кристаллизации. Затем осадок отсасывают на воронке Бюхнера и сушат на воздухе. Выход – 7 г. 2,4,6-Триброманилин – бесцветное кристаллическое вещество; растворим в эфире, хлороформе; не растворяется в воде; Tплав. = 119-120 0C; Tкип. = 300 0C.
Углеводороды
|
|
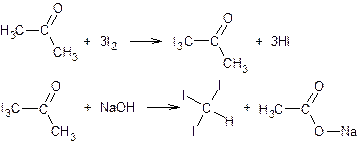
 KBr + H2SO4 → KHSO4 + HBr
KBr + H2SO4 → KHSO4 + HBr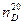 = 1, 4239.
= 1, 4239.