|
|
К72. Печеночная недостаточность.K72.0. Острая и подострая печеночная недостаточность. K72.1. Хроническая печеночная недостаточность. K72.9. Печеночная недостаточность неуточненная.
Печеночная недостаточность - комплекс симптомов, характеризуемый нарушением одной или нескольких функций печени, появляющийся вследствие повреждения ее паренхимы (синдром гепатоцеллюлярной или печеночно-клеточной недостаточности). Портосистемная или печеночная энцефалопатия - это симптомокомплекс нарушений ЦНС, возникающий при печеночной недостаточности с глубоким нарушением многочисленных жизненно важных функций печени. Смертность от печеночной недостаточности составляет 50-80%. При острой печеночной недостаточности возможно развитие печеночной энцефалопатии, которая при острых болезнях печени встречается редко, но летальность может достигать 80-90%.
Этиология и патогенез
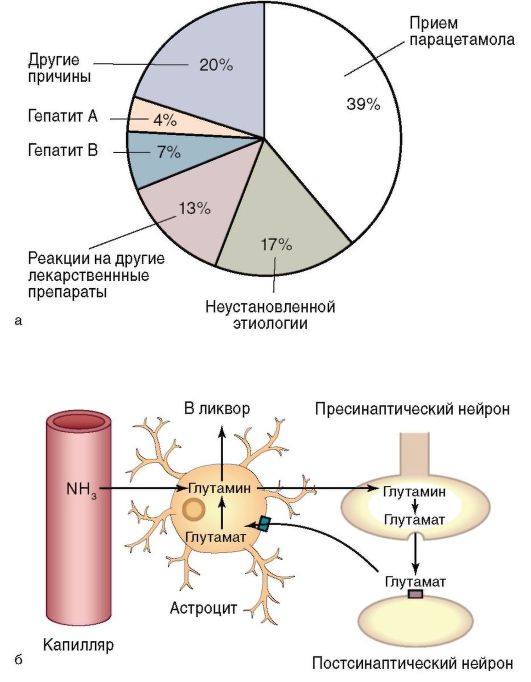
Острая печеночная недостаточность возникает при тяжелых формах вирусных гепатитов А, В, С, D, Е, G, отравлениях гепатотропными ядами (алкоголем, некоторыми лекарственными препаратами, промышленными токсинами, микотоксинами и афлатоксинами, углекислым газом и др.). Ее причинами могут быть вирусы герпеса, цитомегаловирус, вирус инфекционного мононуклеоза, простого и опоясывающего лишая, Коксаки-вирус, возбудитель кори; септицемия при абсцессах печени. Описана острая печеночная недостаточность при токсических гепатозах (синдроме Рея, состоянии после отключения тонкой кишки), болезни Вильсона- Коновалова, синдроме Бадда-Киари. Синдром Бадда-Киари (код по МКБ-10 - I82.0) развивается вследствие прогрессирующего сужения или закрытия печеночных вен. На почве тромбофлебита пупочной вены и аранциева протока, впадающего в устье левой печеночной вены, синдром Бадда-Киари может начаться в раннем детстве. В результате в печени развивается застой со сдавлением печеночных клеток. Синдром Рея (код по МКБ-10 - G93.7) - острая энцефалопатия с отеком мозга и жировой инфильтрацией печени, возникающая у ранее здоровых новорожденных, детей и подростков (чаще в возрасте 4 - 12 лет), связанная с предшествующей вирусной инфекцией (например, ветряной оспой или гриппом типа А) и приемом препаратов, содержащих ацетилсалициловую кислоту. Хроническая печеночная недостаточность является следствием прогрессирования хронических заболеваний печени (гепатитов, цирроза печени, злокачественных опухолей печени и др.). Основные этиологические факторы указаны на рис. 6-17, а. В основе патогенеза печеночной недостаточности лежат два процесса. Во-первых, выраженная дистрофия и распространенный некробиоз гепатоцитов ведут к значительному снижению функций печени. Во-вторых, из-за многочисленных коллатералей между воротной и полой веной значительная часть всосавшихся токсических продуктов поступает в большой круг кровообращения в обход печени. Отравление вызывают необезвреженные продукты распада белка, конечные продукты обмена веществ (аммиак, фенолы). Возникновение печеночной энцефалопатии при печеночной недостаточности связано с нарушениями гомеостаза, кислотно-основного состояния и электролитного состава крови (дыхательным и метаболическим алкалозом, гипокалиемией, метаболическим ацидозом, гипонатриемией, гипохлоремией, азотемией). В системный кровоток из ЖКТ и печени поступают церебротоксические вещества: аминокислоты и продукты их распада (аммиак, фенолы, меркаптаны); продукты гидролиза и окисления углеводов (молочная, пировиноградная кислоты, ацетон); продукты нарушенного метаболизма жиров; ложные нейротрансмиттеры (аспарагин, глутамин), которые оказывают токсические эффекты на ЦНС. Механизм поражения ткани головного мозга связан с нарушением функции астроцитов, которые составляют примерно 30% клеток головного мозга. Астроциты играют ключевую роль в регуляции проницаемости гематоэнцефалического барьера, в обеспечении транспорта нейротрансмиттеров к нейронам головного мозга, а также в разрушении токсических веществ (в частности, аммиака) (рис. 6-17, б).
Рис. 6-17. Хроническая печеночная недостаточность и печеночная энцефалопатия: а - этиология печеночной недостаточности; б - механизм формирования печеночной энцефалопатии
Обмен аммиака. У здоровых людей в печени аммиак трансформируется в мочевую кислоту в цикле Кребса. Он необходим в реакции превращения глутамата в глутамин, которая опосредована ферментом глутаматсинтетазой. При хроническом поражении печени количество функционирующих гепатоцитов уменьшается, создавая предпосылки для гипераммониемии. При возникновении портосистемного шунтирования аммиак, минуя печень, попадает в системный кровоток - возникает гипераммониемия. Аммиак, поступая в головной мозг, приводит к нарушению функционирования астроцитов, вызывая в них морфологические изменения. В результате при печеночной недостаточности возникает отек головного мозга, повышается внутричерепное давление. В условиях цирроза печени и портосистемного шунтирования возрастает активность глутаматсинтетазы скелетной мускулатуры, где начинает происходить процесс разрушения аммиака. Этим объясняется уменьшение мышечной массы у пациентов с циррозом печени, что, в свою очередь, также способствует гипераммониемии. Процессы метаболизма и экскреции аммиака происходят и в почках.
Клиническая картина
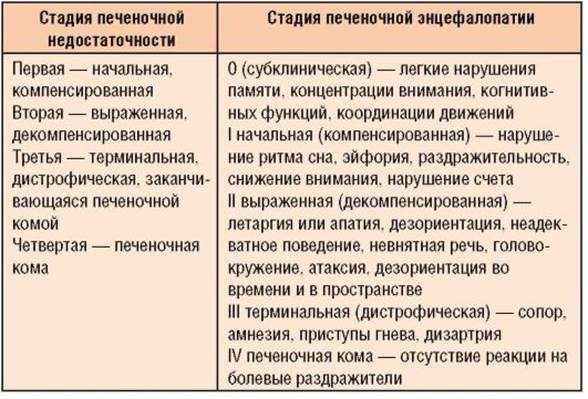
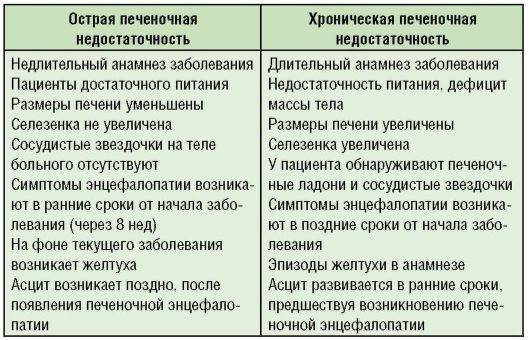
Клиническая картина проявляется расстройствами сознания и когнитивных функций, сонливостью, монотонной речью, тремором, дискоординацией движений. Особенно важными признаками являются быстрое уменьшение размеров печени, ее размягчение и болезненность при пальпации. В табл. 6-14 кратко сведены клинические проявления по стадиям печеночной недостаточности и энцефалопатии, различия острой и хронической печеночной недостаточности - в табл. 6-15.
Таблица 6-14. Классификация стадий печеночной недостаточности и энцефалопатии
Таблица 6-15. Дифференциальная диагностика острой и хронической печеночной недостаточности
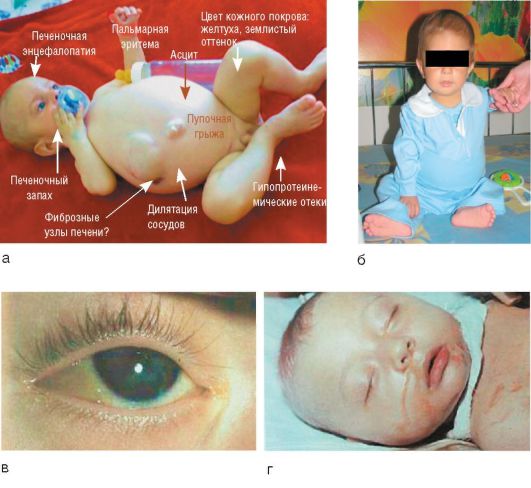
Печеночной коме предшествует общее возбуждение, которое переходит в угнетение сознания: ступор и сопор, затем происходит полная его потеря. Появляются менингеальные явления, патологические рефлексы (хватательный, сосательный), двигательное беспокойство, судороги. Дыхание становится аритмичным, по типу Куссмауля или Чейна-Стокса. Пульс малый, неритмичный. Изо рта и от кожи исходит печеночный запах (foetor hepatica), обусловленный выделением метилмеркаптана; усиливаются желтуха и геморрагический синдром, нарастают асцит, гипопротеинемические отеки (рис. 6-18, а). Клинические проявления декомпенсированной и терминальной стадий ярко представлены на рис. 6-18, б-г. Термином «злокачественная форма» (наиболее тяжелая форма) обозначается качественно новое клиническое состояние, возникающее у больных вирусным гепатитом В в случае развития у них массивного или субмассивного некроза печени.
Рис. 6-18. Печеночная недостаточность: а - клинические проявления; а и б - декомпенсированная стадия; в - терминальная стадия («плавающее глазное яблоко»); г - печеночная кома
В течение последующих 2-3 дней развивается глубокая печеночная кома. Иногда кома наступает, минуя стадию возбуждения.
Диагностика
Проводят лабораторно-инструментальные исследования. • В общем анализе крови выявляются анемия, лейкоцитоз, тромбоцитопения, повышение СОЭ. • При биохимическом исследовании диагностируются билирубинемия, азотемия, гипоальбуминемия, гипохолестеринемия, возрастают уровни АЛТ, АСТ, ЩФ, снижаются уровни фибриногена, калия, натрия, протромбиновый индекс, отмечается метаболический ацидоз. • При УЗИ, КТ печени выявляется изменение размеров и структуры паренхимы печени.
Патоморфология
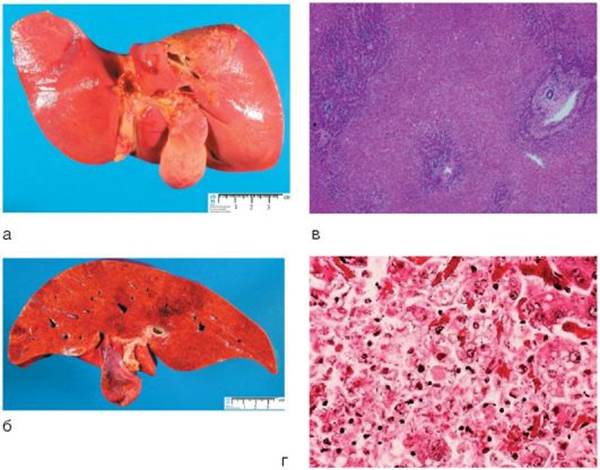
Морфологические изменения в печени касаются всех ее тканевых компонентов: паренхимы, ретикулоэндотелия, соединительнотканной стромы, в меньшей степени - желчевыводящих путей. Различают три варианта острой формы болезни: - острую циклическую форму; - холестатический (перихолангиолитический) гепатит; - массивный некроз печени. Выраженность морфологических изменений зависит от тяжести и этиологии болезни (рис. 6-19, а, б). В разгар заболевания преобладают альтернативные, экссудативные процессы, в период выздоровления - процессы пролиферации и регенерации.
Рис. 6-19. Некроз печени, макро- и микропрепараты: а - этиология неизвестна; б - аденовирусная этиология; в - χ 250; г - χ 400 (окраска гематоксилин-эозином)
При холестатическом (перихолангиолитическом) гепатите морфологические изменения касаются в основном внутрипеченочных желчных ходов (холангиолит и перихолангиолит). Некроз печени представляет собой крайнюю степень изменений в печени, который может быть массивным, когда гибнет почти весь печеночный эпителий или сохраняется незначительная кайма клеток по периферии долек, или субмассивным, при котором некробиозу подвергаются большинство гепатоцитов, преимущественно в центре долек (рис. 6-19, в, г).
|
|