|
|
Адсорбция на поверхности раздела твердое вещество — газ.Адсорбция газа на твердом теле является простейшим случаем адсорбционного процесса, так как система состоит всего из двух компонентов. Конкретный пример такой адсорбции мы рассмотрели в предыдущем параграфе. Опыт показывает, что при прочих равных условиях для твердого адсорбента и данного адсорбируемого газа количество адсорбируемого вещества будет возрастать по мере увеличения адсорбирующей поверхности. Следовательно, чтобы достигнуть большого адсорбционного эффекта, необходимо иметь как можно большую поверхность поглотителя. Способность адсорбента к поглощению газов определяется не только его пористостью, но и физическим состоянием; так, адсорбенты в аморфном состоянии лучше адсорбируют газы, чем в кристаллическом. В качестве адсорбентов на практике применяют древесный и костяной угли, силикагель, высокодисперсные металлы, полученные восстановлением их из оксидов. Активированный уголь как адсорбент применяется в противогазах, а также для очистки воздуха на промышленных предприятиях, для осветления различных растворов и т. п. Высокая адсорбционная способность активированного угля объясняется, сильно развитой поверхностью. Так,, суммарная поверхность всех пор, заключающихся в 1 г такого угля, составляет от 300 до 1000 м2. Такая огромная площадь обусловливает возникновение большого молекулярного силового поля и, стало быть, избыток поверхностной энергии на границе уголь — газ. За счет свободной поверхностной энергии и происходит адсорбция газа, т. е. повышение его концентрации в поверхностном слое угля при одновременном понижении концентрации газа в окружающем пространстве. Как показали исследования, время пребывания молекул газа на поверхности твердого адсорбента очень мало: они удерживаются на адсорбенте всего сотые и тысячные доли секунды и, десорбируясь, замещаются на новые частицы. В конечном итоге устанавливается динамическое равновесие между свободными и адсорбированными молекулами. Скорость достижения адсорбционного равновесия для разных газов неодинакова: при адсорбции СО2 на угле равновесие наступает через 20 с, при адсорбции О2— через 2,5 ч, при адсорбции N2— через 20 ч и т. п. Скорость адсорбции имеет большое значение для практического использования различных адсорбентов. Например, в широко используемом при химической защите противогазе проходящий через коробку воздух должен очень быстро очищаться от примесей отравляющих веществ. Это возможно лишь при высоких скоростях адсорбционных процессов. Активированный уголь в противогазе играет роль не только адсорбента целого ряда отравляющих веществ, но и катализатора реакции разложения многих из них. В качестве примера можно указать на каталитический гидролиз фосгена
или хлорпикрина
Опыт показывает, что адсорбция зависит не только от природы поглотителя, но и от природы поглощаемого газа, при прочих равных условиях сильнее адсорбируются те газы, которые легче конденсируются в жидкость. Следовательно, они обладают более высокой температурой кипения в сжиженном состоянии. Для объяснения явлений адсорбции существуют различные теории. Одна из них — физическая теория, согласно которой природа адсорбционных сил чисто физическая и связана с проявлением межмолекулярных сил. Согласно химической теории ненасыщенные силы адсорбционных поверхностных слоев являются химическими (валентными) силами. Известно несколько теорий физической адсорбции, из которых интерес представляет теория мономолекулярной адсорбции Ленгмюра (1915). В построении ее ученый опирался на представление об адсорбционных силах, которые впервые были высказаны русским ученым Л. Г. Гуревичем. Основные положения теории Ленгмюра: 1. Адсорбция вызывается валентными силами или силами остаточной химической валентности. 2. Адсорбция происходит не на всей поверхности адсорбента, а лишь на активных центрах этой поверхности. Такими центрами являются углубления и выступы, имеющиеся на любой, даже самой гладкой поверхности. Действие таких центров сводится к высокой ненасыщенности их силового поля, благодаря чему центры удерживают газовые молекулы. Причем активность центра тем выше, чем меньше насыщена молекула или атом адсорбента. 3. Адсорбционные силы обладают малым радиусом действия, вследствие чего каждый активный центр адсорбирует лишь одну молекулу адсорбтива, и на адсорбенте образуется мономолекулярный слой адсорбтива. 4. Адсорбированные молекулы газа не сидят прочно на поверхности адсорбента; они непрерывно обмениваются с молекулами в газовой сфере, при этом устанавливается динамическое адсорбционное равновесие. Каждая молекула задерживается в течение короткого времени на поверхности, затем в результате флуктуации энергии молекулы отрываются от активного центра, уступая место новой молекуле. В отличие от физической адсорбции химическая адсорбция, или хемосорбция, осуществляется при помощи химических сил. Эти виды адсорбции имеют следующие отличительные признаки: физическая адсорбция — явление обратимое, и теплота ее составляет всего 8,4—33,5 кДж/моль, в то время как теплота химической адсорбции достигает десятков и сотен кДж/моль. С повышением температуры физическая адсорбция уменьшается, а химическая увеличивается. Объясняется это тем, что химическая адсорбция требует более значительной энергии активации (40—120 кДж/моль). Химическая адсорбция необратима, поэтому процесс десорбции состоит не в простом отрыве адсорбированной молекулы, а в разложении поверхностного химического соединения. В качестве типичного примера химической адсорбции можно назвать адсорбцию кислорода на поверхности угля. Весьма характерным является то, что при нагревании с поверхности адсорбента удаляется не кислород, а окись углерода. Согласно современным представлениям при адсорбции проявляются все виды физических и химических сил, т. е. адсорбция, по существу, является физико-химическим процессом. И действительно, советские ученые Н. А. Шилов, М. М. Дубинин, Л. К. Лепинь установили, что при различных случаях адсорбции играют роль физические и химические взаимодействия между адсорбентом и адсорбируемым веществом. Это особенно четко проявляется при адсорбции газов. Исследования показали, что при поглощении первых порций газа на чистой поверхности адсорбента чаще проявляется действие химических сил, а при последующей адсорбции газа, при повышении давления процесс переходит постепенно в чисто физический.
Изотермы адсорбции.
Как видно из рис. 5.2, повышение давления газа Рис 5.2 увеличивает адсорбируемое количество его. Однако на разных участках изотермы адсорбции это влияние сказывается неодинаково . Наиболее сильным оно оказывается в области низких давлений, где адсорбция подчиняется закону Генри для растворимости газов в жидкостях, т. е. она прямо пропорциональна давлению газа. Дальнейшее повышение давления тоже увеличивает количество адсорбированного газа, но уже во все уменьшающейся степени. И, наконец, при достаточно высоких давлениях кривая стремится к прямой, параллельной оси абсцисс. В этом случае достигнуто полное насыщение адсорбента и повышение давления газа уже не влияет на его адсорбцию. Таким образом, между адсорбцией и давлением (концентрацией) газа отсутствует прямая пропорциональная зависимость. Это и вызвало необходимость найти математическое выражение, которое достаточно точно описало бы экспериментальные данные. Впервые эмпирическое уравнение, которым пользуются и в настоящее время, было предложено Фрейндлихом. Это уравнение имеет следующий вид:
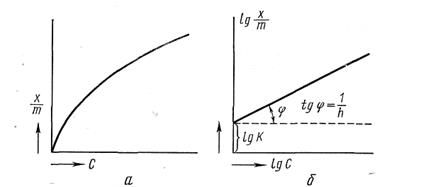
где х/m— величина адсорбции на единицу массы адсорбента; р — равновесное давление газа над поглотителем (для растворов пользуются равновесной концентрацией С), К и 1/n — константы адсорбции, характерные для данного процесса адсорбции в определенных пределах, значение которых можно найти из опытных данных. Рассмотрим, как определяются численные значения констант. На рис. 5.3, а дано графическое изображение уравнения для случая адсорбции из жидкости. По оси абсцисс отложены равновесные концентрации С (кмоль/м3), по оси ординат — значения х/m
Рис 5.3 (кмоль/кг). Если прологарифмировать уравнение (5.3), получим следующее выражение:
из которого можно найти значения постоянных К 1/п. Для этой цели построим график, выражающий зависимость lg х/m — lg С. Получается прямая линия (рис. 5.3 ,б), отсекающая на оси ординат отрезок, равный lg К, а тангенс угла наклона этой прямой к абсциссе дает значение 1/n. Уравнение (5.4) есть уравнение прямой линии. Несмотря на то, что уравнение Фрейндлиха широко применяется на практике, оно имеет определенные недостатки. Многочисленные исследования показали, что значение адсорбции, вычисляемое на основании этого уравнения, не соответствует данным опыта в области малых и больших концентраций. Константы К и 1/n являются чисто эмпирическими и не имеют реального физического смысла. Позднее (1917) Ленгмюр вывел простейшее уравнение адсорбции для случая адсорбции газа на гладкой твердой поверхности (стекло, слюда, монокристаллы), оказавшееся в дальнейшем применимым и к другим поверхностям раздела. При выводе своего уравнения Ленгмюр исходил из допущения, что адсорбционный слой мономолекулярен, т. е. только один слой молекул связан силами молекулярного сцепления с поверхностью. При этом указанный слой полностью поглощает собой все адсорбционные силы поверхности адсорбента, поэтому образование второго слоя адсорбированных молекул исключается. Число активных мест поверхности ученый принял равным единице, а долю активных мест, связанных с адсорбированными молекулами, обозначил через х. При этом условии свободная часть поверхности равняется 1—х. Обозначив величину адсорбции через Г и учитывая, что при х=0, Г = 0 и при х=1, Г = Г∞, он нашел, что х=Г/Г∞, где Г — количество вещества, адсорбированное единицей поверхности при полном насыщении. Тогда уравнение Ленгмюра можно записать:
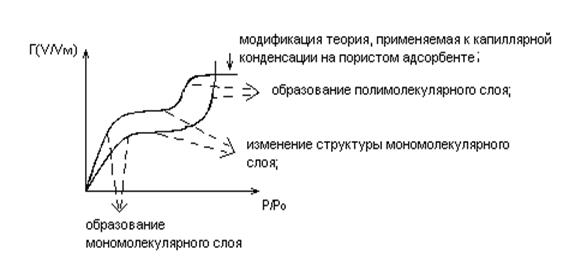
Опыт показывает, что уравнение изотермы адсорбции Ленгмюра сравнительно удовлетворительно дает количественную характеристику адсорбции при низких и при высоких концентрациях поглощаемого вещества. В отличие от уравнения изотермы Фрейндлиха все величины, входящие в уравнение Ленгмюра, имеют определенный физический смысл и вполне обоснованы теоретически. Уравнение Ленгмюра исходит из расчета мономолекулярного адсорбционного слоя. Однако не все ученые разделяют эту точку зрения. По мнению Поляни и ряда других авторов, возможен многослойный адсорбционный слой, причем эта точка зрения имеет некоторое теоретическое и опытное обоснование. По теории Ленгмюра молекулы адсорбтива, притянутые к отдельным активным точкам, между собой не взаимодействуют. Однако при накоплении в адсорбционном слое молекул веществ, обладающих высокой молекулярной массой, между ними могут возникнуть значительные силы сцепления. В этом случае уравнение Ленгмюра дает неверные результаты. В ряде случаев, в частности при применении пористых адсорбентов, таких, как уголь, силикагель и др., формула Фрейндлиха дает лучшие результаты, чем уравнение Ленгмюра. Изотерма Брунауэра – Эммета – Теллера (БЭТ) см. рис.5.4. Теория адсорбции БЭТ исходит из: 1) адсорбционный слой имеет непостоянную толщину на поверхности адсорбента; 2) тепловой эффект адсорбции ≠ тепловому эффекту конденсации адсорбтива; 3) центры адсорбции – двумерные ячейки на поверхности адсорбента; 4) латеральное взаимодействие отсутствует.
Рис. 5.4 При малых P/P0 изотерма БЭТ переходит в изотерму Ленгмюра. Достоинство: 1)учитывает полимолекулярность слоя адсорбтива. Недостатки: 1) не учитывает латеральные взаимодействия. На основе БЭТ – изотермы рассчитывают величину адсорбции для конкретных систем.
|
|
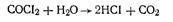

 Как показали исследования, адсорбция увеличивается с ростом давления (концентрации) газа, однако это увеличение не беспредельно. Для каждого адсорбируемого газа (при t = const) через некоторое время над адсорбентом устанавливается предельная величина адсорбции, отвечающая равновесию между обеими фазами. Кривая зависимости адсорбции от давления (концентрации) при постоянной температуре носит название изотермы адсорбции. Она является одной из важнейших характеристик адсорбционных процессов. На рис. 5.2 изображены типичные изотермы адсорбции СО2 углем при различных температурах, взятые из работы А. А. Титова.
Как показали исследования, адсорбция увеличивается с ростом давления (концентрации) газа, однако это увеличение не беспредельно. Для каждого адсорбируемого газа (при t = const) через некоторое время над адсорбентом устанавливается предельная величина адсорбции, отвечающая равновесию между обеими фазами. Кривая зависимости адсорбции от давления (концентрации) при постоянной температуре носит название изотермы адсорбции. Она является одной из важнейших характеристик адсорбционных процессов. На рис. 5.2 изображены типичные изотермы адсорбции СО2 углем при различных температурах, взятые из работы А. А. Титова.