|
|
Растворимость веществ в воде
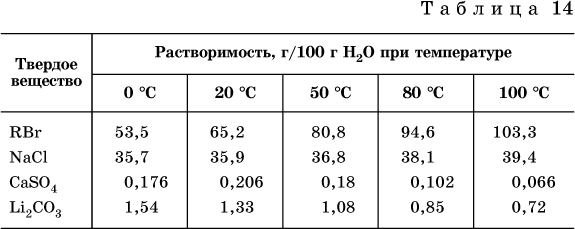
Раствор – это гомогенная система, состоящая из двух или более веществ, содержание которых можно изменять в определенных пределах без нарушения однородности. Водные растворы состоят из воды (растворителя) и растворенного вещества. Состояние веществ в водном растворе при необходимости обозначается нижним индексом (р), например, KNO3 в растворе – KNO3(p). Растворы, которые содержат малое количество растворенного вещества, часто называют разбавленными, а растворы с высоким содержанием растворенного вещества – концентрированными. Раствор, в котором возможно дальнейшее растворение вещества, называется ненасыщенным, а раствор, в котором вещество перестает растворяться при данных условиях, – насыщенным. Последний раствор всегда находится в контакте (в гетерогенном равновесии) с нерастворившимся веществом (один кристалл или более). В особых условиях, например при осторожном (без перемешивания) охлаждении горячего ненасыщенного раствора твердого вещества, может образоваться пересыщенный раствор. При введении кристалла вещества такой раствор разделяется на насыщенный раствор и осадок вещества. В соответствии с химической теорией растворов Д. И. Менделеева растворение вещества в воде сопровождается, во‑первых, разрушением химических связей между молекулами (межмолекулярные связи в ковалентных веществах) или между ионами (в ионных веществах), и, таким образом, частицы вещества смешиваются с водой (в которой также разрушается часть водородных связей между молекулами). Разрыв химических связей совершается за счет тепловой энергии движения молекул воды, при этом происходит затрата энергии в форме теплоты. Во‑вторых, попав в воду, частицы (молекулы или ионы) вещества подвергаются гидратации. В результате образуются гидраты – соединения неопределенного состава между частицами вещества и молекулами воды (внутренний состав самих частиц вещества при растворении не изменяется). Такой процесс сопровождается выделением энергии в форме теплоты за счет образования новых химических связей в гидратах. В целом раствор либо охлаждается (если затрата теплоты превосходит ее выделение), либо нагревается (в противном случае); иногда – при равенстве затраты теплоты и ее выделения – температура раствора остается неизменной. Многие гидраты оказываются настолько устойчивыми, что не разрушаются и при полном выпаривании раствора. Так, известны твердые кристаллогидраты солей CuSO4 5Н2O, Na2CO3 • 10Н2O, KAl(SO4)2 • 12Н2O и др. Содержание вещества в насыщенном растворе при Т = const количественно характеризует растворимость этого вещества. Обычно растворимость выражается массой растворенного вещества, приходящейся на 100 г воды, например 65,2 г КBr/100 г Н2O при 20 °C. Следовательно, если 70 г твердого бромида калия ввести в 100 г воды при 20 °C, то 65,2 г соли перейдет в раствор (который будет насыщенным), а 4,8 г твердого КBr (избыток) останется на дне стакана. Следует запомнить, что содержание растворенного вещества в насыщенном растворе равно, в ненасыщенном растворе меньше и в пересыщенном растворе больше его растворимости при данной температуре. Так, раствор, приготовленный при 20 °C из 100 г воды и сульфата натрия Na2SO4 (растворимость 19,2 г/100 г Н2O), при содержании 15,7 г соли – ненасыщенный; 19.2 г соли – насыщенный; 2O.3 г соли – пересыщенный. Растворимость твердых веществ (табл. 14) обычно увеличивается с ростом температуры (КBr, NaCl), и лишь для некоторых веществ (CaSO4, Li2CO3) наблюдается обратное. Растворимость газов при повышении температуры падает, а при повышении давления растет; например, при давлении 1 атм растворимость аммиака составляет 52,6 (20 °C) и 15,4 г/100 г Н2O (80 °C), а при 20 °C и 9 атм она равна 93,5 г/100 г Н2O.
В соответствии со значениями растворимости различают вещества: – хорошо растворимые, масса которых в насыщенном растворе соизмерима с массой воды (например, КBr – при 20 °C растворимость 65,2 г/100 г Н2O; 4,6М раствор), они образуют насыщенные растворы с молярностью более чем 0,1М; – малорастворимые, масса которых в насыщенном растворе значительно меньше массы воды (например, CaSO4 – при 20 °C растворимость 0,206 г/100 г Н2O; 0,015М раствор), они образуют насыщенные растворы с молярностью 0,1–0,001М; – практически нерастворимые, масса которых в насыщенном растворе пренебрежимо мала по сравнению с массой растворителя (например, AgCl – при 20 °C растворимость 0,00019 г на 100 г Н2O; 0,0000134М раствор), они образуют насыщенные растворы с молярностью менее чем 0,001М. По справочным данным составлена таблица растворимости распространенных кислот, оснований и солей (табл. 15), в которой указан тип растворимости, отмечены вещества, не известные науке (не полученные) или полностью разлагающиеся водой. Условные обозначения, используемые в таблице: «р» – хорошо растворимое вещество «м» – малорастворимое вещество «н» – практически нерастворимое вещество «–» – вещество не получено (не существует) « » – вещество смешивается с водой неограниченно
Примечание. Данная таблица отвечает приготовлению насыщенного раствора при комнатной температуре путем внесения вещества (в соответствующем агрегатном состоянии) в воду. Следует учесть, что получение осадков малорастворимых веществ с помощью реакций ионного обмена возможно не всегда (подробнее см. 13.4).
|
|