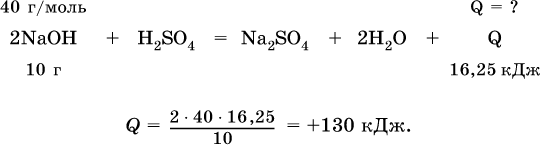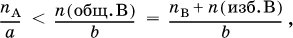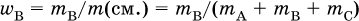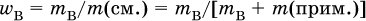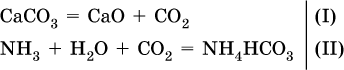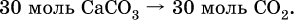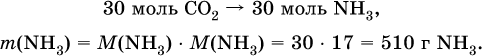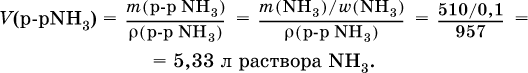|
|
Пример решения задачи части В
Вычислите тепловой эффект (кДж) реакции полной нейтрализации гидроксида натрия серной кислотой, если в расчете на 10 г щелочи выделяется 16,25 кДж теплоты.
Задания для самостоятельного решения части А
1. В реакции между железом и хлором на 11,2 л (н.у.) окислителя приходится выделение 132 кДж теплоты, следовательно, в расчете на 0,5 моль железа выделится количество теплоты (кДж), равное 1) +198 2) +148,5 3) +99 4) +49,5
2. Триоксид серы массой 280 г вносят в воду, протекает реакция с тепловым эффектом +73 кДж. Количество теплоты (кДж) в условиях опыта равно 1) +204,4 2) +255,5 3) +408,8 4) +511
3. Термическое разложение нитрата калия привело к выделению 4,48 л (н.у.) газа. Тепловой эффект реакции равен ‑282 кДж, следовательно, сопровождающее процесс количество теплоты (кДж) составляет 1) ‑56,4 2) ‑112,8 3) ‑225,6 4) ‑282
4. Сожжено 10 л (н.у.) аммиака на воздухе (тепловой эффект реакции +1532 кДж). По условию опыта количество теплоты составит 1) +171 2) +342 3) +766 4) +855
5. Термическое разложение карбоната кальция с тепловым эффектом ‑179 кДж привело к получению 33,6 г твердого остатка. В этих условиях поглощенное количество теплоты (кДж) равно 1) ‑537 2) ‑214,8 3) ‑375,9 4) ‑107,4
6. При термическом разложении дихромата аммония протекает экзотермическая реакция, в которой на 1,4 моль образовавшейся воды приходится +106 кДж; следовательно тепловой эффект реакции (кДж) равен: 1) +505 2) +404 3) +303 4) +606
7. Реакция сгорания угарного газа в кислороде сопровождается экзо‑эффектом +566 кДж. Количество теплоты (кДж), приходящееся на 224 г угарного газа, равно 1) +1132 2) +2264 3) +283 4) +566
8. Тепловой эффект реакции полного сгорания ацетилена в кислороде равен +2596 кДж. При сгорании 2 л (н.у.) этого газа выделяется количество теплоты (кДж) 1) +29 2) +58 3) +116 4) +232
9. В термическом разложении метана с образованием ацетилена и 560 л (н.у.) водорода тепловой эффект реакции равен ‑376 кДж. Количество поглощенной теплоты (кДж) в условиях опыта составляет 1) ‑2256 2) ‑752 3) ‑1128 4) ‑376
10. При полном сгорании бутадиена‑1,3 в кислороде на 0,5 моль затраченного окислителя выделяется +18 кДж теплоты, следовательно, на 0,5 моль вступившего в реакцию алкадиена приходится количество теплоты (кДж), равное 1) +49,5 2) +99 3) +148,5 4) +198
Масса (объем, количество вещества) продукта по реагенту в избытке или с примесями
Избыток и недостаток реагентов. Количества, массы и объемы (для газов) реагентов не всегда берутся стехиометрическими, т. е. в соответствии с уравнениями реакции. Чаще один из реагентов берется в избытке, а следовательно, другой реагент оказывается в недостатке. Избыток реагента участвовать в реакции не будет. Для реакции aA + bB = cC + dDопределение реагентов, взятых в избыткеи в недостатке, проводят по неравенству (А – в недостатке, В – в избытке):
где n(общ. В) – общее (взятое с избытком) количество реагента В, пB – стехиометрическое (необходимое для реакции) количество В, n(изб. В) – избыточное количество В, причем
n(изб. B) = n(общ. B) – nB.
Внимание! Расчет получаемых количеств (масс, объемов) продуктов проводят по реагенту в недостатке. Степень чистоты вещества. Химические вещества никогда не бывают идеально чистыми, они всегда содержат в себе примеси. Массовая доля вещества В в смеси, например А + В + С, – это отношение массы вещества В к массе смеси:
Сумма массовых долей всех веществ смеси равна 1 (100 %). Если в смеси примесь присутствует в следовом (неопределяемом) количестве, то говорят о практически чистом веществе. Когда же в веществе имеется примесь в заметном (определяемом) количестве, то само вещество называют основным (его количество преобладает), а другое вещество – это и есть примесь. Степень чистоты основного вещества В – это массовая доля этого вещества в навеске с определенной массой:
Природные вещества (минералы, руды) всегда содержат заметное количество примеси (примесей).
Пример решения задачи
Углекислый газ поглощается 10 %‑ным раствором аммиака (плотность раствора 957 г/л) с образованием кислой соли. Предварительно СO2 получают термическим разложением 5 кг известняка СаСO3 (степень чистоты 60 %). Установите взятый объем (в литрах) раствора аммиака. Элементы ответа. 1) Составлены уравнения реакций:
2) Установлено количество основного вещества в известняке:
и количество углекислого газа по уравнению (I):
3) Установлена масса затраченного аммиака по уравнению (II):
4) Установлен объем взятого раствора аммиака:
Задания для самостоятельного решения частей В, С
1. К 100 г 10 %‑ного раствора хлорида кальция добавили 100 г 10 % – ного раствора AgNO3. Найдите массу (в граммах) осадка. 2. Смешали горячие растворы, содержащие по 33 г хлорида алюминия и сульфида калия. Установите объем (в литрах, н.у.) выделившегося газа. 3. Какой объем (в литрах, н.у.) хлора можно получить при взаимодействии 2 моль хлороводорода (взят в виде соляной кислоты) и 3 моль оксида марганца(IV)? 4. Через раствор, приготовленный из 2 г смеси NaCl + Nal и 100 мл воды, пропустили 1 л (н.у.) хлора. Затем раствор выпарили и сухой остаток нагрели. Получили 1,78 г твердого вещества. Рассчитайте массовую долю (в %) хлорида в исходном растворе. 5. Вычислите объем (в литрах, н.у.) газа, полученного действием кипящей H2SO4 (конц.) на 292,5 г хлорида натрия, содержащего 2O% инертных примесей. 6. После прокаливания 50 г минерала тенорит (CuО и инертные примеси) в токе водорода образуется металл и конденсируется вода объемом 8,1 мл. Определите степень чистоты (в %) этого минерала. 7. Установите массу (кг) технического алюминия (степень чистоты 98 %), требуемую для получения 64,22 кг хрома из оксида хрома (III). 8. Прокалили 32,1 г хлорида аммония с 55,5 г гидроксида кальция (содержит 20 % инертных примесей). Рассчитайте объем (в литрах, н.у.) собранного газа. 9. К 285 г нитрата натрия (содержит примесь хлорида магния) добавили раствор избытка нитрата серебра (I). Выпал осадок массой 86,1 г. Вычислите степень чистоты (в %) нитрата натрия. 10. Найдите массовую долю (в %) примеси NaHCO3 в образце технической соды Na2CO3, если после нагревания 10 г образца получено 9,69 г твердого остатка. 11. Смешали 20 г уксусной кислоты и 8,4 г питьевой соды NaHCO3. Определите объем (в литрах, н.у.) газа, собранного после окончания реакции. 12. На гидрирование 250 г смеси Cl7Н33СООН + Cl7Н35СООН затратили 16,8 л (н.у.) газа. Установите массовую долю (в %) предельной карбоновой кислоты в исходной смеси.
|
|