|
|
ЛИНЕЙЧАТЫХ СПЕКТРОВ ИСПУСКАНИЯС ПОМОЩЬЮ МОНОХРОМАТОРА УМ-2 Цель работы: познакомиться с устройством монохроматора УМ-2 и использованием его для определения длины волны спектральных линий. Приборы и принадлежности: монохроматор УМ-2, конденсор, ртутная лампа с источником питания, неоновая лампа, лазер.
Сведения из теории Тела, нагретые до достаточно высоких температур, светятся, т.е. излучают электромагнитные волны в видимой области спектра. Излучение, обусловленное нагреванием, называется тепловым. Тепловое излучение является самым распространенным в природе (все тела, имеющие температуру больше 0 К, излучают). Осуществляется тепловое излучение за счет энергии теплового движения атомов и молекул вещества. Но свечение вещества, в частности газа, может быть вызвано и другими способами. Например, электрическим разрядом в газах при низком давлении, когда взаимодействия атомов нет, а излучение происходит за счет подводимой электрической энергии. Пропуская излучение какого-либо тела через прибор, осуществляющий его разложение в спектр, можно судить по характеру спектра о присутствии в излучении той или иной длины волны, а также оценивать распределение энергии по участкам спектра. Спектры, полученные таким образом, называютсяспектрами испускания. Пары и газы, находящиеся в атомарном состоянии, при нагревании или электрическом разряде дают линейчатые спектрыиспускания, состоящие из относительно узких “линий” т.е. узких частотных интервалов. Каждое вещество (газ) имеет свой, только ему присущий спектр (количество линий и их длины волн). Так, водород в видимой области спектра имеет четыре линии, ртуть - десять и т.д. Пары, образованные из молекул (молекулярный газ), дают полосчатыйспектр: линии излучения представляют собой широкие полосы сложного строения. Твердые тела при нагревании дают сплошной спектр с неравномерным распределением энергии по длинам волн (по частотам). Линейчатые спектры многих газов можно разделить на группы -серии, в каждой из которых длины волн (частоты) вычисляются по одной сравнительно простой формуле. Так, швейцарский физик Бальмер показал, что частоты линий водорода видимой и ближайшей ультрафиолетовой частей спектра могут быть вычислены по формуле
где R- некоторая постоянная, называемая постоянной Ридберга (R= =3,28985×1015 c-1), а n= 3, 4, 5... Аналогичные формулы были получены и для других серий. Оказалось, что все шесть серий спектра водорода могут быть представлены одной формулой - обобщенной формулой Бальмера:
где k в зависимости от серии имеет значения 1,2,3,4, ...; n - целое число, принимающее значение в каждой серии, начиная с k+1, т.е. n= k+1, k+2, k+3,... . Закономерности положения линий в атомарных спектрах могут быть объяснены только на основе квантовых представлений, базирующихся на постулатах Бора. 1. Атомы могут длительное время находиться в так называемых стационарныхсостояниях, когда, несмотря на происходящее в них ускоренное движение электронов, атомы не излучают и не поглощают энергию. Стационарные состояния характеризуются дискретным рядом значений энергии E1, E2, ... Eк , ... En ,... 2. Стационарными являются те состояния, для которых момент импульса электрона, движущегося по круговой орбите, кратен величине h/2p. L = m v r = n h /2p,(11.3)
где m- масса электрона; v - его скорость; r- радиус орбиты электрона; n = 1,2,3 ...; h- постоянная Планка. 3. Атомы излучают (поглощают) свет при переходе из одного стационарного состояния в другое. Излучение при этом переходе монохроматично, его частота определяется из условия
hn = En - Ek ,(11.4)
где Enи Ek- энергии атома в рассматриваемых состояниях. Теория Бора применима и к водородоподобным атомам, состоящим из ядра с зарядом Zеи одного электрона, вращающегося вокруг него (ионы Не+, Li++ и др.). На основании постулатов Бора можно вычислить для атомов водорода и водородоподобных атомов следующее: а) радиус орбиты r и скорость электрона v в стационарных состояниях:
где m, e - масса и заряд электрона; Z - порядковый номер элемента в таблице Менделеева;e 0 - электрическая поcтоянная, n = 1, 2, 3, ...; б) энергию атома:
в) частоту, излучаемую атомом при переходе из состояния n в состояние k:
что совпадает с эмпирической формулой (11.2), причем для Z= 1 величина
и есть постоянная Ридберга. Формула (11.2) позволяет изобразить графически энергетические уровни атома водорода (горизонтальные линии на рис. 11.1). Стрелками указаны переходы атома водорода, соответствующие излучению различных спектральных линий. Из рисунка видно, что спектральные линии, относящиеся к определенной серии, связаны с переходом атома на данный энергетический уровень с различных более высоких уровней.
Монохроматор УМ-2
Универсальный монохроматор УМ-2 - это оптический прибор, предназначенный для различных спектральных исследований в диапазоне длин волн от 380 до 1000 нм. Оптическая схема прибора изображена на рис.11.2, его общий вид показан на рис.11.3. Свет от источника 7 (рис.11.2), пройдя
Конструктивно монохроматор можно разделить на три части (см. рис.11.3): коллиматор, призменный столик с поворотным механизмом и выходную трубу. Коллиматор состоит из входной щели 5, объектива 4 (см. рис.11.2), затвора 8 (см. рис. 11.3). Ширина входной щели может изменяться от 0 до 4 мм посредством микрометрического винта 7 (см. рис.11.3). При этом изменяется интенсивность прошедшего света и ширина спектральных линий. Затвор 8 служит для перекрытия света, что необходимо делать, если измерения не производятся. Столик 5 с диспергирующей призмой 4 получает движение от микрометрического винта поворотного механизма. На измерительном барабане 10 нанесена винтовая дорожка с делениями. Вдоль дорожки скользит указатель поворота барабана. Отсчет читается против индекса 9, скользящего по спиральной канавке. В выходную трубу входят объектив 2 и щель 1 (см. рис. 11.2). Ширина выходной щели, как и входной, может изменяться с помощью микрометрического винта 2 (см. рис. 11.3). При изучении спектров испускания выходную трубу заменяют зрительной трубой 11, снабженной сменными окулярами и указателем, с которым совмещают ту или иную спектральную линию при оценке ее положения. Зрительную трубу закрепляют с помощью винта 1 (рис. 11.3). Монохроматор превращается при этом в спектроскоп.
Выполнение работы 1. Градуировка монохроматора 1.1. Познакомиться (путем осмотра) с устройством монохроматора, уяснить назначение отдельных его узлов, проверить наличие других необходимых приборов и принадлежностей. 1.2. Подключить блок питания к сети, кнопкой “пуск” зажечь ртутную лампу. Свет лампы с помощью линзы (см. рис.11.2) сфокусировать на входную щель. 1.3. Вращая барабан, просмотреть через зрительную трубу (без каких-либо замеров) весь спектр, сопоставляя увиденное с табл. 11.1. Отрегулировать ширину входной щели и зрительную трубу так, чтобы спектральные линии были достаточно узкими и четкими (две желтые линии должны быть видны раздельно). Барабан установить в крайнее положение (от себя). 1.4. Проградуировать монохроматор: установить, какое деление барабана соответствует той или иной линии спектра. Рекомендуется начинать с красных линий (j®), затем то же самое повторить от фиолетовых линий (показания барабана j). Результаты (j и j®) записать в табл. 11.1. 1.5. Вычислить средние значения <j> и по данным табл. 11.1 построить график <j> = f (l). Таблица 11.1
2.Определение длин волн линий спектра неоновой лампы 2.1.Ртутную лампу на оптической скамье заменить на неоновую.
2.2. Пункты 1.2 и 1.3 повторить с неоновой лампой (кнопкой “пуск” сейчас не пользоваться). 2.3. Определить деления барабана монохроматора (см. п. 1.4), соответствующие хорошо видимым линиям спектра неоновой лампы. Результаты записать в табл. 11.2. Таблица 11.2
2.4. Вычислить средние значения <j> для отдельных линий и, воспользовавшись графиком (см. п. 1.5), определить длины волн линий спектра неона. П р и м е ч а н и е: при наличии лазера определить длину волны лазерного излучения.
КОНТРОЛЬНЫЕ ВОПРОСЫ
1. Какими способами можно вызвать свечение вещества? 2. Что такое спектры испускания? Виды этих спектров. 3. Что такое “серия” линий линейчатого спектра? Привести примеры. 4. Сформулировать постулаты Бора. 5. Как на основе постулатов Бора объяснить происхождение линейчатых спектров и “серий” линий в частности? 6. Какие задачи для атомов водорода решены по теории Бора? 7. Назначение, оптическая схема и устройство монохроматора. 8. Что значит проградуировать монохроматор? Как это сделать? 9. Как с помощью градуировочной кривой определить длины волн “неизвестных” спектральных линий? ЛАБОРАТОРНАЯ РАБОТА № 12 ОПРЕДЕЛЕНИЕ ПОСТОЯННОЙ ПЛАНКА С ПОМОЩЬЮ СВЕТОДИОДА Цель работы:познакомиться с одним из методов определения постоянной Планка. Приборы и принадлежности:светодиод с экраном, выпрямитель, вольтметр, оптическая скамья, дифракционная решетка, масштабная линейка.
|
|
 , (11.1)
, (11.1) , (11.2)
, (11.2) , (11.5)
, (11.5) ; (11.6)
; (11.6) , (11.7)
, (11.7)

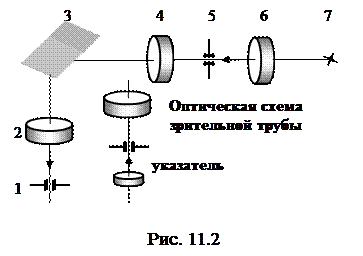 через конденсор 6, падает на входную щель 5 монохроматора. Объектив 4 делает пучок света параллельным (щель 5 располагается в передней фокальной плоскости объектива 4). Далее свет падает на переднюю грань дисперсионной призмы 3. Так как свет разной длины волны отклоняется призмой на разные углы (дисперсия), то из призмы свет разных длин волн выходит по различным направлениям. Лучи, направленные вдоль оси объектива 2, собираются в его фокальной плоскости, в которой находится выходная щель 1 монохроматора. При вращении призмы 3 (вокруг оси, перпендикулярной плоскости рисунка, см. рис.11.2) линии спектра будут смещаться относительно щели 1, и, таким образом, легко добиться того, чтобы выделялась та или иная линия.
через конденсор 6, падает на входную щель 5 монохроматора. Объектив 4 делает пучок света параллельным (щель 5 располагается в передней фокальной плоскости объектива 4). Далее свет падает на переднюю грань дисперсионной призмы 3. Так как свет разной длины волны отклоняется призмой на разные углы (дисперсия), то из призмы свет разных длин волн выходит по различным направлениям. Лучи, направленные вдоль оси объектива 2, собираются в его фокальной плоскости, в которой находится выходная щель 1 монохроматора. При вращении призмы 3 (вокруг оси, перпендикулярной плоскости рисунка, см. рис.11.2) линии спектра будут смещаться относительно щели 1, и, таким образом, легко добиться того, чтобы выделялась та или иная линия.
