|
|
Электролитпен коагуляциялау кинетикасы 15 главаКрафт нүктесі қатты кристалдық жағдайдағы және мицеллярлы ерітіндідегі БАЗ энергияларының қатынасымен анықталады. Мицеллярлы ерітінділердің энергиясы әр түрлі жағдайларда аз өзгереді, мысалы қарсыионның табиғатына байланысты, сонымен қатар орналасу параметрлеріне байланысты да кристалдық күйдің энергиясы күрт өзгеруі мүмкін. Крафт құбылысын түсіну үшін, орналасу эффектісі және қатты денедегі иондардың электростатикалық әсерлесуі эффектілерін қарастыру қажет. Егер БАЗ ерігіштігі өте аз болса, онда оның практикалық маңызы жоқ. Әдетте ұзын тізбекті БАЗ-дар әдетте тиімдірек болғандықтан, БАЗ-дардың молекулалық дизаинындағы нәзік балансты сақтау керек. Крафт нүктесін әдетте қатты БАЗ-дың күйін өзгерту арқылы төмендетуге болады. Қарсы ионның өзгеруі қатарында гидрофобты тізбектердің кеңістікті орналасу ерекшеліктерін ескеру қажет. Крафт нүктесі төмен БАЗ-ды жасап шығару әдетте қатты күйдегі тізбектердің орналасу тиімділігін азайтуға негізделген. Бұл үшін келесі тәсілдерді қолданады: 1) тізбектерді тармақтандыру үшін метилдік топтарды немесе басқа да алмастырғыштарды енгізу; 2) алкилдік тізбектерге қосбайланыстарды енгізу; 3) алкилдік тізбек пен иондық топ арасына полярлы сигменттер (әдетте оксиэтиленді топтар) енгізу. Осы жалпы принциптерді кермек сумен араласатын БАЗ-дың өндірісінде қолданады. Тізбектердің «балқуын» қадағалау биологиялық жүйелер, соның ішінде биомембраналар үшін өте маңызды және ол қанықпаған көмірсутекті тізбектерді реттеумен жүзеге асады.
4.4 Электролиттің әсері. БАЗ ерітіндісіндегіқоспалар, әcipece электролиттер МТДК мәндеріне айтарлықтай әсер етеді. БАЗ ерітіндісіне электролит енгізу келесі нәтижелерге әкеледі: • электролит қосқанда МТДК күрт (ондаған есе) азаяды; • мицелла түзгіш БАЗ-дың көмірсутектітізбeгi ұзарған сайын оның МТДК мәніне электролиттің тигізетінәcepi күшейеді; • ионсыз БАЗ-дардың МТДК мәндеріне электролиттер айтарлықтай әсер етпейді. БАЗ-дардың МТДК мәндерін спирттер елеулі азайтады. Суға қарағанда спирттің полярлығы төмен болғандықтан оларерітндімен мицеллалардың арасында таралады. Спирт молекуласындағы көмірсутекті радикал неғұрлым ұзын болса, соғұрлым оның мицелла құрамына кіру қабілеті арта түседі. Осының салдарынан мицелла түзуіне жеткілікті БАЗ молекулаларының (иондарының) саны (агрегаттық саны), яғни МТКК мәні азаяды.
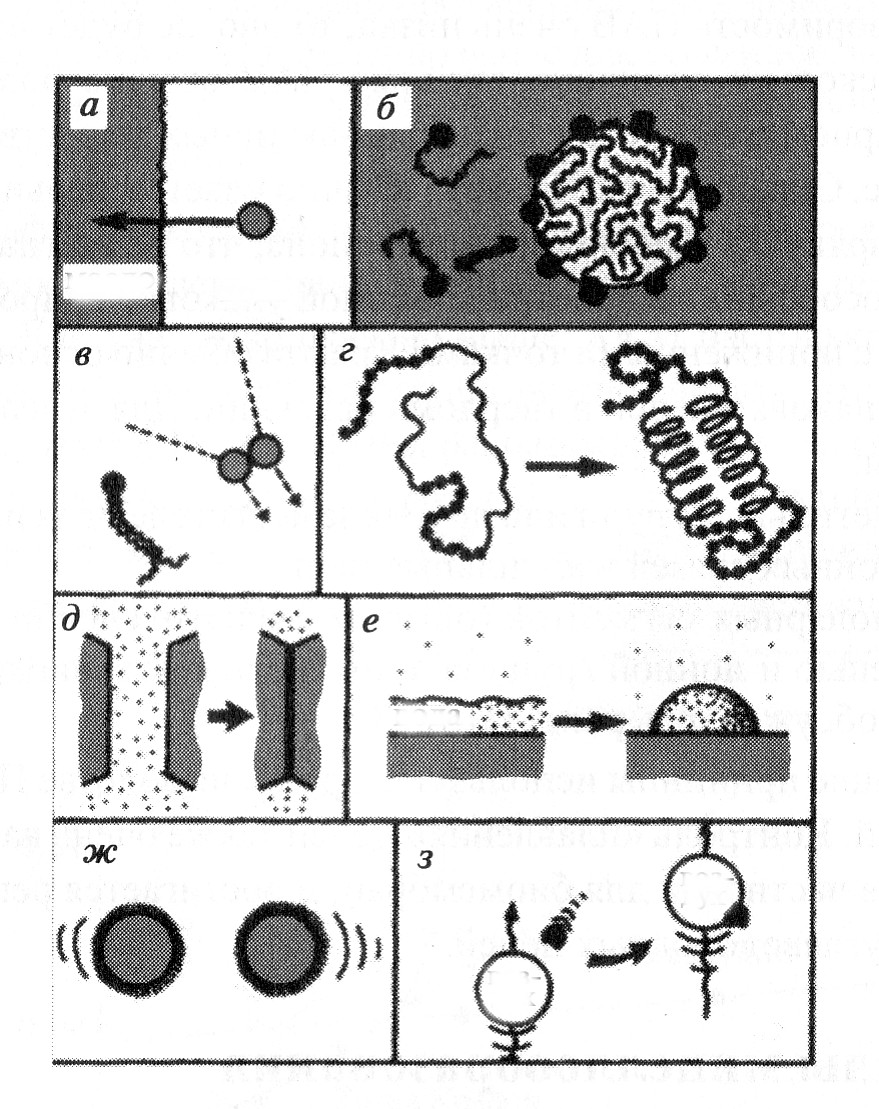
5. Мицеллатүзілудің қозғаушы күштері және термодинамикалық модельдері 5.1 Гидрофобтық әрекеттесулер Осыған дейін БАЗ-дар мен полярлы липидтердің дифильділіктері олардың сипаттамалары ретінде айтылып келді. Судың гидрофобтық топтармен әрекеттесуі тиімсіз болып табылады. Бұл оларды сулы ортадан итеріп шығару қозғаушы күшін тудырады, бұған фазаларды макроскопиялық бөлу немесе полярлы емес топтарды басқа бір әдіспен «жасыру» нәтижесінде қол жеткізуге болады. Гидрофобтық эффектер мен гидрофобтық әрекеттесулердің көптеген көріністері белгілі (8-сурет).
8-сурет. Гидрофобтық әрекеттесулермен қадағаланатын, яғни су мен полярлы емес молекулалар немесе полярлы емес беттер арасындағы қатынасты болдырмауға ұмтылатын құбылыстар: а – су мен май бір-бірімен араласпайды, бірақ бұл жерде судан көмірсутек молекулаларын ығыстырып шығаратын күшті қозғаушы күш пайда болады; б – БАЗ молекулаларының өздік ұйымдасуы; в – көмірсутек тізбектерінің ассоциациясының басқа типтері; г –белоктар фолдингі; д – полярлы емес беттердің судағы күшті адгезиясы; е –гидрофобтық беттердің суда жұқпауы; ж – гидрофобтық бөлшектердің судағы жылдам коагуляциясы; з – гидрофобтық бөлшектердің ауа көпіршіктеріне жабысуы (көбікті флотацияның механизмі).
Судағы көмірсутек молекулаларына, оны көмірсутек фазасына немесе кез-келген басқа полярлы емес ортаға ауыстыруға ұмтылатын күш әсер етеді. Егер көмірсутек молекуласына полярлық топты енгізсек, фазаларға макроскопиялық бөлуге кедергі келтіретін қарама-қарсы күш пайда болады. Егер бұл күш көп емес болса, бөлу жүре береді. Егер ол гидрофобтық эффекттен көп болса, онда дифильдік зат молекулалық еріген болып қала береуі мүмкін немесе кішкентай агрегаттар, мысалы димерлер түрінде бола алады. БАЗ-дардың өздігінен ассоциациялануы әрқашанда гидрофобтық және гидрофильдік әрекеттесулердің балансымен байланысты болады. Гидрофобтық әрекеттесулер алканның алкилдік тізбегі немесе БАЗ-дардың гидрофобтық тобы өскен сайын күшейеді. Молекуладағы көміртегі атомының саны өскен сайын алкандардың ерігіштігінің төмендеуімен БАЗ-дардың МТКК-нің өзгеруінің арасында белгілі бір коррелеция болады. Сонымен мицеллатүзілуді фазаларға бөлу мен комплекстердің түзілуі арасындағы аралық құбылыс ретінде қарастыруға болады; бұл термодинамика тұрғысынан қарағандағы мицеллатүзілуді модельдеуде көрінеді. Мицеллатүзілуді келесі модельдердің біреуінің тұрғысынан қарастырады.
5.2. Фазалық бөлу моделі
Бұл модельде мицеллатүзілу жаңа (жалған) фаза, ал МТДК – ерітіндінің молекулалық БАЗ-бен қанығу концентрациясы болып табылатын фазалық бөлуге ұқсас үдеріс ретінде қарастырылады. Ендеше БАЗ-дың МТДК-дің артық мөлшері тек мицелланың концентрациясына ғана әсер етеді. Мицеллатүзілудің бұл моделі тәжірибелік мәліметтерді өңдеу үшін қолайлы. Физика-химиялық өлшеулер нәтижесінде БАЗ молекулаларының әртүрлі жағдайларда бола алатын орташа өлшемі алынады (<Q(pmik,paq>). МТДК-дан төмен концентрацияда БАЗ-дың тек жеке молекулалары ғана болады және Q-дің орташа мәні тең:
<Q> = Qaq МТДК-дан жоғары концентрация үшін Cmic=Ctot-МТДК және Сaq=МТДК екенін ескере отырып, мынадай өрнек аламыз: <Q>-pmicQmic+paqQaq=(1+MTДK/Ctot)Qmic+(MTДK/Ctot)Qaq МТДК едәуір жоғары концентрациялар үшін <Q> Qmic –ға жақындайды. Фазалық бөлу моделі оны қолданған кезде қиындықтар туғызбайды, ол көрнекті және көптеген жүйелерді сипаттау үшін жарамды. Ол мицелладағы БАЗ-дардың агрегация саны неғұрлым жоғары болған сайын, соғұрлым жақсы орындалады.
5.3. Массалар әрекеттесу заңына негізделген модель Мицеллярлық комплекс An, БАЗ-дың мономерлі А1 формасымен тепе-теңдікте болсын делік: nA1 ↔An (An)/(A1)n=K К-тепе-теңдік константасы. Бұл модельге сәйкес агрегация сандарын МТДК-ға маңындағы Qбқ өзгерістерінен алуға болады. Жүйенің өзгерісі неғұрлым баяу жүрген сайын, соғұрлым агрегация саны аз болады және бұндай жүйені сипаттау үшін массалар әрекеттесу заңына негізделген модель фазалық бөлу моделінен гөрі көбірек қолданылады. Мицеллалардың құрамына кіретін БАЗ-дардың үлесінің БАЗ-дардың жалпы концентрациясына тәуелділігі агрегация сандары N өте көп болғанда, бұл тәуелділіктерде күрт көтерілу байқалатынын және бұл жердегі өзгеріс фазалық бөлу моделіндегідей болатынын көрсетті. Шын мәнінде мицеллалар монодисперстік емес, себебі әрқашанда агрегация сандары бойынша қандай да бір таралу болады және мицеллалар біртіндеп түзіледі, мұны келесі модель ескереді. 5.4. Көптеген тепе-теңдіктер моделі
2A1↔A2 A2+A1↔A3 A3+A1↔A4 • • • An-1+A1↔An (An)/(An-1A1)=Kn Берілген тепе-теңдіктер иондық емес БАЗ-ды сипаттайды. Қарсыиондардың мицеллалармен ассоциациясын ескеру үшін, қарсыиондар үшін тепе-теңдікті жазу қажет. Бұл негізінен ең дұрыс жол емес, себебі тепе-теңдік константаларымен жұмыс жасау, белгілі бір комплекстер түзумен жүретін аз арақашықтықта жұмыс жасау дегенді білдіреді. Қарсыиондардың таралуы үлкен арақашықтықтарда жүретін электростатикалық әрекеттесулермен бақыланады. Сондықтан мицеллалармен байланысқан қарсыиондарға белгілі бір сипаттама беру мүмкін емес. Бірақ бұл қарсыиондардың немесе олардың ассоциацияларының мицелламен байланысы физикалық мағынасын жоғалтады деген емес. Сонымен мәліметтерді талдағанда сәйкес модельдердің шектеулеріне мән берген жөн. Өздік диффузия коэффициенттері әртүрлі орталар (мицеллярлы, молекулярлы) бойынша орташа есептелген өлшемдер болып табылады, сондықтан
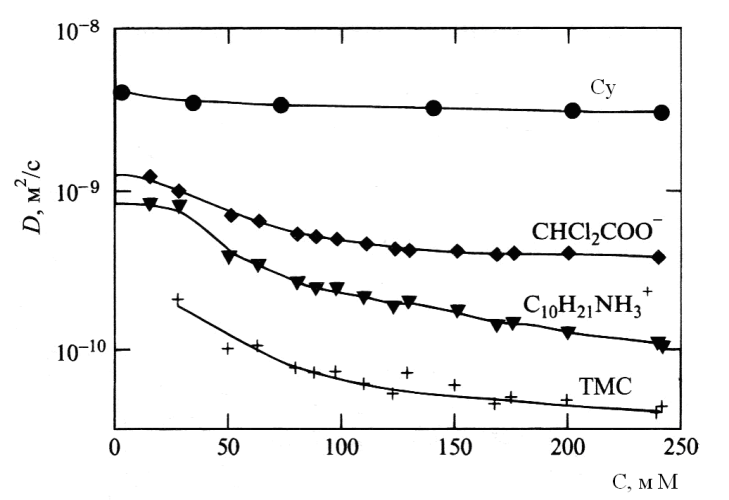
Dobs=pmicDmic+pfreeDfree немесе Dobs=(CmicDmic+CfreeDfree)/Ctot мұнда р, D және С бар жерлерді сәйкесінше белгілі бір аймақтағы молекула үлесі, өздік диффузия коэффициенті және концентрацияны белгілейді. Dfree мәнін МТДК аз кездегі С қатысындағы өлшемдерден анықтайды, ал молекулалары мицеллаға біріккен үлгілер үшін Dmic. 9-суретте көрсетілген зерттеулерде мицеллатүзілу үрдісіне әсер етпес үшін нашар еритін тетраметилсиланның (ТМС) төмен концентрциялары қолданылған. Мицеллалар үлкен қосылыстар болып табылатындықтан, олардың өздік диффузия коэффициенті молекулалық еріген БАЗ-дардың сәйкес өлшемдерінен көп аз болып келеді. 9-суретте көрсетілгендей әр түрлі молекулалардың өздік диффузия коэффициенттері бір-бірінен МТКК-дан жоғары БАЗ-дар концентрациялары қатысында өте ерекшеленеді. Судың молекулалары мицеллалармен ең аз ассоциацияланған, ал ТМС молекулалары мицеллада көп дәрежеде локализделген. БАЗ-дар диффузиясы мен қарсыиондардың диффузиясын өлшеуден алынған сандық талдау нәтижелері 10-суретте көрсетілген. Ионды БАЗ-дың мицеллатүзілуіне тән кейбір маңызды заңдылықтарды атап өтуге болады. Олар: - Жақсы жақындаулар арқылы МТДК-дан төмен БАЗ-дың барлық молекулалары молекулалық еріген күйде болады деп есептеуге болады. - МТДК-дан жоғары концентрацияларда молекулалық еріген БАЗ концентрациясы азаяды және МТДК-дан көп кіші мәндерге жетуі мүмкін. - Бос қарсыиондардың концентрациясы МТДК-дан төмен БАЗ-дың концентрациясы өскен сайын, МТДК-дан жоғары концентрациялардағыға қарағанда артады. - Мицелламен байланысқан қарсыиондармен БАЗ-дың мицелладағы қатынастары қарсыиондардың байланысу дәрежесін анықтайды: β=Cmicc/Cmics.
9-сурет. БАЗ (дециламмоний), қарсыион (дихлорацетат), су молекуласы мицеллардың өздік диффузия коэффициенттерінің БАЗ-дың жалпы концентрациясына тәуелділігі.
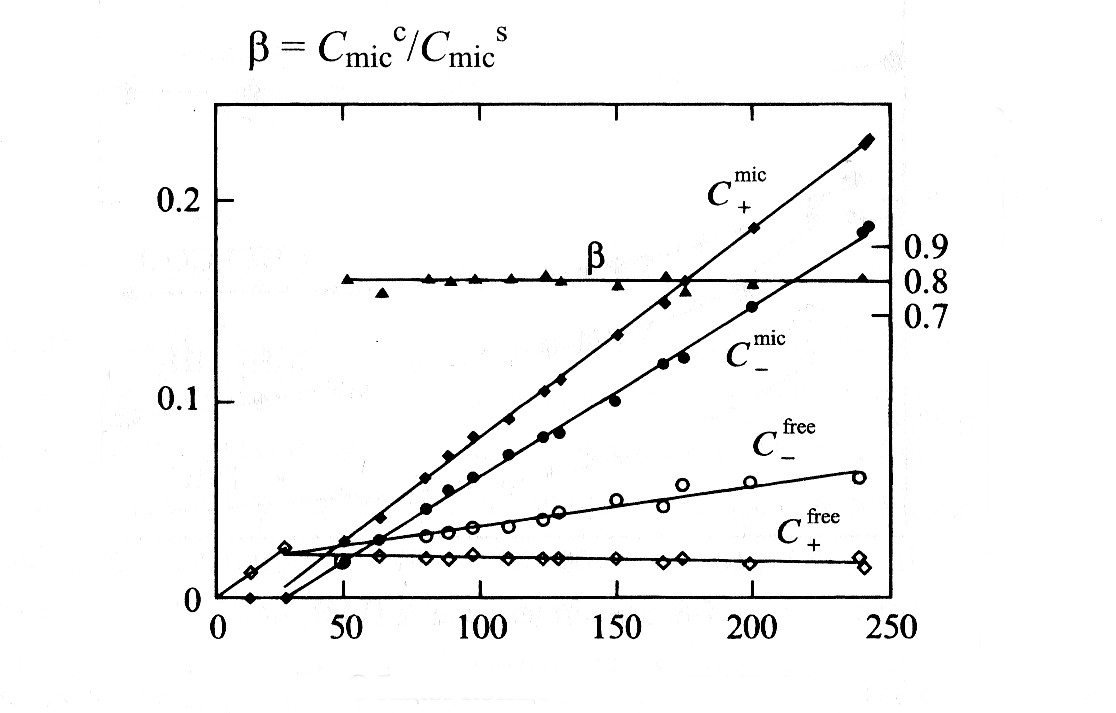
10-сурет. БАЗ-дың жалпы концентрациясынан мицелланың және БАЗ-дың бос иондарының (+), қарсы иондардың (-) концентрацияларының тәуелділігі.
Мицеллалық концентрация бірнеше реттілікке өскен сайын β тұрақты болып қала береді. Әдетте мұны қарсыиондардың мицелладағы конденсациясымен түсіндіреді. Бұл мицелламен қарсыионның ассоциациясы мицелланың зарядының эффективті тығыздығын қамтамасыз ететін белгілі бір деңгейге дейін өседі, ал содан кейін тұрақты болып қалады. Бұл жағдайларда қарсыиондардың мицелламен концентрациясы мицелланың концентрациясына тәуелсіз, сонымен бірге енгізілетін электролит концентрациясы температураға тәуелсіз. Қарсыиондардың конденсация құбылысы кез-келген электростатикалық теория тұрғысынан жақсы түсіндірілетін зарядталған беттер мен полиэлектролиттерді қоса алғандағы жүйелер үшін тән құбылыс. |
|